
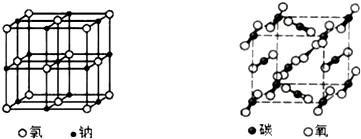
| A. | 两种晶体内均含有共价键 | B. | 构成两种晶体的微粒均是原子 | ||
| C. | 两者的硬度、熔沸点差别较大 | D. | 两种晶体均属于离子晶体 |
分析 A.氯化钠为离子晶体,只存在离子键;
B.氯化钠为离子晶体,构成晶体的微粒是阴、阳离子,二氧化碳为分子晶体,构成晶体的微粒是分子;
C.离子晶体的硬度、熔沸点较大,分子晶体的硬度、熔沸点较小;
D.氯化钠为离子晶体,二氧化碳为分子晶体.
解答 解:A.氯化钠为离子晶体,只存在离子键,二氧化碳为分子晶体,只存在共价键,故A错误;
B.氯化钠为离子晶体,构成晶体的微粒是阴、阳离子,二氧化碳为分子晶体,构成晶体的微粒是分子,而不是原子,故B错误;
C.离子晶体的硬度、熔沸点较大,分子晶体的硬度、熔沸点较小,所以两者的硬度、熔沸点差别较大,故C正确;
D.氯化钠为离子晶体,二氧化碳为分子晶体,而不是全部是离子晶体,故D错误;
故选C.
点评 本题主要考查了不同晶体组成、性质差异,难度不大,注意一般离子晶体的熔沸点大于分子晶体.


科目:高中化学 来源: 题型:推断题
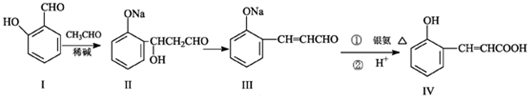
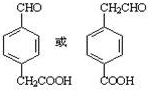 .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 ;
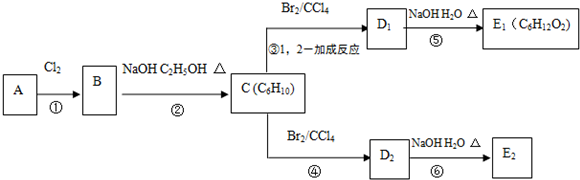
;
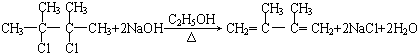
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
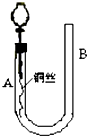 为了说明稀硝酸与铜反应产生无色的一氧化氮气体,某同学设计了如图所示的实验装置.实验时,将分液漏斗的活塞打开,从U形管的长管口B注入稀硝酸,一直到U形管的短管口A单孔塞下沿且液面不再留有气泡为止.关闭活塞,并用酒精灯在U形管短管下微热.当铜丝上有气泡产生时,立即撤去酒精灯.试回答:
为了说明稀硝酸与铜反应产生无色的一氧化氮气体,某同学设计了如图所示的实验装置.实验时,将分液漏斗的活塞打开,从U形管的长管口B注入稀硝酸,一直到U形管的短管口A单孔塞下沿且液面不再留有气泡为止.关闭活塞,并用酒精灯在U形管短管下微热.当铜丝上有气泡产生时,立即撤去酒精灯.试回答:查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | X-、Y-、Z-、W-中Z-还原性最强 | B. | X2、Y2、Z2、W2中Z2的氧化性最强 | ||
| C. | 2Z-+Y2═-+Z2不能向右进行 | D. | 还原性X->Y- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有②④ | B. | 只有①⑤⑥ | C. | 只有②④⑥ | D. | 只有③⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com