
 µŚ1¾ķµ„ŌŖŌĀæ¼ĘŚÖŠĘŚÄ©ĻµĮŠ“š°ø
µŚ1¾ķµ„ŌŖŌĀæ¼ĘŚÖŠĘŚÄ©ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®a% | B£®2a% |
| C£®1~1.75a% | D£®1~0.75a% |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Ęū³µÅŷŵēóĮæĪ²Ęų |
| B£®Éś²śĮņĖį¹¤³§ÅŷŵÄĪ²Ęų |
| C£®¹¤ŅµÉĻ“óĮæŗ¬ĮņČ¼ĮĻµÄČ¼ÉÕ |
| D£®ĀŅæ³ĄÄ·„£¬ĘĘ»µĮĖÉśĢ¬Ę½ŗā |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®½šŹōÄĘÓėĄäĖ®·“Ó¦£ŗNa+2H2O====Na++2OH-+H2”ü |
| B£®Ģ¼ĖįøĘĶ¶Čė“×ĖįČÜŅŗÖŠCaCO3+2CH3COOH====Ca2++2CH3COO-+H2O+CO2”ü |
| C£®ĻņCa(ClO)2ČÜŅŗÖŠĶعżĮæCO2ĘųĢå£ŗCa2++2ClO-+CO2+H2O====CaCO3”ż+2HClO |
D£®ĻņĮņĖįĶČÜŅŗÖŠµĪČėBa(OH)2ČÜŅŗ£ŗBa2++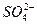 ====BaSO4”ż ====BaSO4”ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ŗģÉ«ĻČ¼ÓÉīŗóĶŹÖĮĪŽÉ« | B£®ŗģÉ«Į¢æĢĶŹČ„£¬ČÜŅŗ±äĪŖĪŽÉ« |
| C£®ŗģÉ«¼ÓÉī£¬ŃÕÉ«²»ĶŹ | D£®ŗģÉ«¼Č²»¼ÓÉīŅ²²»ĶŹČ„ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®H2SO4 | B£®°±Ė® | C£®NaOH | D£®HNO3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā

| A£®øĆ·“Ó¦ÖŠÅØĮņĖį±ķĻÖĮĖĒæŃõ»ÆŠŌŗĶĖįŠŌ |
| B£®¢ŚÖŠŃ”ÓĆĘ·ŗģČÜŅŗŃéÖ¤SO2µÄÉś³É |
| C£®¢ŪÖŠŃ”ÓĆNaOHČÜŅŗĪüŹÕ¶ąÓąµÄSO2 |
| D£®ĪŖČ·ČĻCuSO4Éś³É£¬Ļņ¢ŁÖŠ¼ÓĖ®£¬¹Ū²ģŃÕÉ« |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®bmol | B£®amol | C£®a/2 mol | D£®3a/2mol |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com