
| A. | 加入过量的KI溶液充分反应后,Kw(AgCl)减小 | |
| B. | 加入过量的KI溶液充分反应后,溶液中Ag+和I-的浓度之积等于Ksp(AgI) | |
| C. | 加入过量的KI溶液充分反应后,溶液中Ag+和Cl-的浓度之积等于Ksp(AgCl) | |
| D. | Ksp(AgI)<Ksp(AgCl) |
分析 氯化银的溶解性大于碘化银,向AgCl饱和溶液中加入KI溶液,碘离子和银离子会结合为更难溶的碘化银沉淀,则Ksp(AgI)<Ksp(AgCl),以此解答该题.
解答 解:A.加入过量的KI,AgCl转化为AgI,则说明Ag+和Cl-的浓度之积等小于Ksp(AgCl),Kw(AgCl)减小,故A正确;
B.AgI的饱和溶液中Ag+和I-的浓度之积等于Ksp(AgI),故B正确;
C.生成AgI沉淀,不存在AgCl,说明溶液中Ag+和Cl-的浓度之积小于Ksp(AgCl),故C错误;
D.氯化银的溶解性大于碘化银,白色沉淀转化为黄色沉淀.故Ksp(AgI)<Ksp(AgCl),故D正确.
故选C.
点评 本题考查了沉淀溶解平衡的分析判断,为高频考点,侧重于学生的分析能力的考查,注意溶度积常数是温度的函数,沉淀可以实现沉淀转化,题目难度中等.


 初中暑期衔接系列答案
初中暑期衔接系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al3+ NH4+ Br- SO42- | B. | Na+ Fe2+ Cl- NO3- | ||
| C. | K+ Ba2+ Cl- NO3- | D. | K+ Na+ SO42- SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
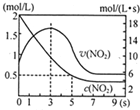 氮及其化合物在工业生产和国防建设中有广泛应用.回答下列问题:
氮及其化合物在工业生产和国防建设中有广泛应用.回答下列问题: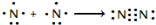 .
.| 化学键 | N-H | N-N | N═N | N≡N | O═O | O-H |
| 键能(kJ/mol) | 390.8 | 193 | 418 | 946 | 497.3 | 462.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com