
| 催化剂 |
| 催化剂 |
| 3 |
| 2 |
| 1 |
| 2 |
| A、a-1/2 | ||
B、
| ||
| C、a1/2 | ||
| D、a-2 |
科目:高中化学 来源: 题型:
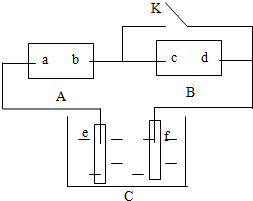 如图A为直流电源,B为浸透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽,接通电路后,发现B 上的 C 点显红色,请填空:
如图A为直流电源,B为浸透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽,接通电路后,发现B 上的 C 点显红色,请填空:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+ Na+ OH- Cl- |
| B、Mg2+ Na+ SO42- OH- |
| C、H+ Na+ Cl- CO32- |
| D、Ba2+ Cu2+ Cl- SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,pH=7的CH3COONa与CH3COOH的混合溶液中离子浓度大小顺序为c(Na+)=c(CH3COO-)>c(H+)=c(OH-) |
| B、将pH=10的氨水稀释后,溶液中所有离子的浓度均降低 |
| C、中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量前者小于后者 |
| D、常温下,同浓度的Na2CO3溶液与NaHCO3溶液相比,Na2CO3溶液的pH较大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若氨水中c(OH-)=0.1mol?L-1则混合溶液中c(H+)=c(OH-) | ||
| B、若a=0.1则混合溶液中c(H+)=c(Cl-) | ||
| C、若c(NH4+)+c(H+)=c(Cl-)+c(OH-)则一定有a=0.1 | ||
D、若混合后溶液中c(H+)=c(OH-)=10-7mol?L-1则常温下氨水的电离常数为
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、凡是放热反应都是自发的,凡是吸热反应都是非自发的 |
| B、自发反应熵一定增大,非自发反应熵一定减小或不变 |
| C、要判断反应进行的方向,必须综合考虑体系的焓变和熵变 |
| D、自发反应在任何条件下都能实现 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、化学变化的实质是旧键的断裂和新键的生成,有物质变化但不一定有能量变化 |
| B、氢气的燃烧热为285.8kJ?mol-1,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l)△H=285.8kJ?mol-1 |
| C、Ba(OH)2?8H2O(s)+2NH4Cl(s)=BaCl2(s)+2NH3(g)+10H2O(l)△H<0 |
| D、已知中和热为57.3kJ?mol-1,若将含0.5molH2SO4的浓溶液与含1molNaOH的溶液混合,放出的热量要大于57.3kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com