
(分)A、B、C、D、E、F六种元素(前20号元素)的核电荷数依次增大。C是地壳中含量最高的元素;D的最高价氧化物的水化物分别能与E、F的最高价氧化物的水化物反应;E原子的最外层电子数是其最内层电子数的3倍;F元素是化学肥料中一种重要元素,其原子的次外层电子数与倒数第三层的电子数相等;A与F具有相同的最外层电子数;B元素的某种单质常作为干电池中的电极材料。试回答下列问题:
(1)由A、B两元素按原子个数之比为1︰1组成的某分子,其相对分子质量小于30,请写出实验室制备该物质的化学反应方程式 。
(2)D、E、F三种元素的原子半径由大到小顺序是 (用元素符号表示)。
(3)由C、D、E、F四种元素组成的某盐,可用作净水剂,也可用于制作膨化食品。该盐的化为 ,将该盐溶液与Ba(OH)2溶液按溶质物质的量之比1:2混合反应,此反应的离子方程式为 。
(1)CaC2 + 2H2O → Ca(OH)2 + C2H2 ↑ (2分)
(2)r(K)>r(Al)>r(S) 或K >Al >S (2分)
(3)KAl(SO4)2 (2分)
Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O (2分)
本题考查原子结构,元素周期律知识;由C是地壳中含量最高的元素,可知C为O;F元素是化学肥料中一种重要元素,其原子的次外层电子数与倒数第三层的电子数相等,则F为K,其最高价氧化物对应的水化物为KOH;B元素的某种单质常作为干电池中的电极材料,可推测B为碳;E原子的最外层电子数是其最内层电子数的3倍,可推测E为O或S,但O 无含氧酸,则E为硫,其最高价氧化物对应的水化物为H2SO4;D的最高价氧化物的水化物能与KOH、H2SO4反应,则D为铝;A与F具有相同的最外层电子数,且可与B按1:1组成分子,可推测A为氢。(1)由A、B按1:1组成的分子,且相对分子质量小于30的分子为C2H2,实验室制取C2H2的化学方程式为CaC2 + 2H2O → Ca(OH)2 + C2H2 ↑ (2)K 、Al 、S原子半径大小关系为: K >Al >S (3)K、Al、S、O组成的净水剂为KAl(SO4)2 ;
该盐溶液与Ba(OH)2溶液按溶质物质的量之比1:2混合反应,Al3+与OH-的物质的量比为1:4,则铝以AlO2-形式存在,反应的离子方程式为 Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O 。


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
(7分,每空1分)A、B、C、D为同一周期的四种元素,原子序数依次增大,已知0.2摩A与酸充分反应时,在标况下可生成2.24升氢气;B的氧化物既可溶于强酸又可溶于强碱溶液;C、D阴离子的电子层结构与氩原子相同,C的气态氢化物与C的低价氧化物反应,又可得到C的单质。试回答:
(1)A、B、C、D的元素符号分别为______、____ 、 、______。
(2)用电子式表示A与C形成化合物的过程:
_________________________________________________。
(3)写出B的氧化物与A的氢氧化物反应的离子方程式:
_________________________________ 。
(4)写出实验室制备D的单质的化学反应方程式:
__________________________________________。
查看答案和解析>>
科目:高中化学 来源:2010年河南省河南大学附中高一上学期期中考试化学卷 题型:单选题
(4分)有A、B、C、D四种可溶性离子化合物,它们的阳离子是Ag+、Na+、Mg2+、Cu2+,阴离子是Cl-、OH-、NO3-、SO42-(每种离子只能用一次)
现将溶液两两混合,记录现象如下:
A+B→白色沉淀;B+ D→白色沉淀;C+D→蓝色沉淀
则(1)A、B、C、D的化学式分别是_________、__________、___________、_________。
(2)分别写出下列反应的离子方程式
A+B→
B+ D→
C+D→
查看答案和解析>>
科目:高中化学 来源:2010—2011年辽宁省沈阳二中高一下学期6月月考化学试卷 题型:填空题
(7分,每空1分)A、B、C、D为同一周期的四种元素,原子序数依次增大,已知0.2摩A与酸充分反应时,在标况下可生成2.24升氢气;B的氧化物既可溶于强酸又可溶于强碱溶液;C、D阴离子的电子层结构与氩原子相同,C的气态氢化物与C的低价氧化物反应,又可得到C的单质。试回答:
(1)A、B、C、D的元素符号分别为______、____ 、 、______。
(2)用电子式表示A与C形成化合物的过程:
_________________________________________________。
(3)写出B的氧化物与A的氢氧化物反应的离子方程式:
_________________________________ 。
(4)写出实验室制备D的单质的化学反应方程式:
__________________________________________。
查看答案和解析>>
科目:高中化学 来源:2010-2011学年山西省高三下学期第一次模拟考试化学试卷 题型:填空题
(13分)现有A、B、C、D、E、F六种化合物,已知它们的阳离子有 ,阴离子有
,阴离子有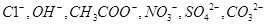 ,现将它们分别配成
,现将它们分别配成 的溶液,进行如下实验:
的溶液,进行如下实验:
① 
 测得溶液A、C、E呈碱性,且碱性为A>E>C;
测得溶液A、C、E呈碱性,且碱性为A>E>C;
② 向B溶液中滴加稀氨水,先出现沉淀,继续滴加氨水,沉淀消失;
③ 
 向D溶液中滴加
向D溶液中滴加 溶液,无明显现象;
溶液,无明显现象;
④ 向F溶液中滴加氨水,生成白色絮状沉淀,沉淀迅速变成灰绿色,最后变成红褐色。

 根据上述实验现象,回答下列问题:
根据上述实验现象,回答下列问题:
(1) 实验②中反应的化学方程式是

 (2)E溶液是
,判断依据是
(2)E溶液是
,判断依据是
(3)写出下列四种化合物的化学式:A 、C
、
 D
、F
。
D
、F
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com