
| A. | Ki1的表达式为Ki1=$\frac{c({H}_{2}C{O}_{3})}{C({H}^{+})•C(HC{{O}_{3}}^{-})}$ | |
| B. | Ki2对应的电离过程是HCO3-+H2O≒H2CO3+OH- | |
| C. | 当碳酸的电离平衡正向移动时,Ki1与Ki2均相应增大 | |
| D. | 改变条件使Ki1减小,则Ki2一定也减小 |
分析 A、Ki1的表达式为Ki1=$\frac{c({H}^{+})c(HC{O}_{3}^{-})}{c({H}_{2}C{O}_{3})}$;
B、Ki2对应的电离过程是HCO3-+H2O≒CO32-+H3O+;
C、Ki1与Ki2是温度的函数;
D、电离过程是吸热过程,要使Ki1减小,只能是降温,所以Ki2一定减小;
解答 解:A、Ki1的表达式为Ki1=$\frac{c({H}^{+})c(HC{O}_{3}^{-})}{c({H}_{2}C{O}_{3})}$,故A错误;
B、Ki2对应的电离过程是HCO3-+H2O≒CO32-+H3O+,而HCO3-+H2O≒H2CO3+OH-,是碳酸氢根离子的水解反应方程式,故B错误;
C、Ki1与Ki2是温度的函数,与反应进行的方向无关,故C错误;
D、电离过程是吸热过程,要使Ki1减小,只能是降温,所以Ki2一定减小,故D正确;
故选D.
点评 本题考查了弱电解质的电离,学生要清楚电离子常数表达式的书写、影响因素是解本题关键,难度中等.


科目:高中化学 来源: 题型:选择题
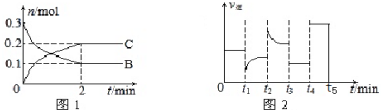
| A. | x=2.反应开始2min内,v(A)=0.05 mol•L-1•min-1 | |
| B. | 若tl时改变的条件是降温,平衡正向移动,则该反应为放热反应 | |
| C. | 若t2时改变的条件是增大c的浓度,则t2时正反应速率减小 | |
| D. | t3-t5时间段B的浓度一定未发生变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定等于0.01 | B. | 一定大于0.01 | ||
| C. | 一定大于或等于0.01 | D. | 可能小于0.01 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 理论上讲,任何自发的氧化还原反应都可以设计成原电池.
理论上讲,任何自发的氧化还原反应都可以设计成原电池.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4 | B. | C3H4 | C. | C2H4 | D. | C4H8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①③④ | C. | ①②④ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  1 mol甲分子内含有10 mol共价键 | |
| B. |  由乙分子构成的物质不能发生氧化反应 | |
| C. |  丙分子的二氯取代产物只有三种 | |
| D. |  分子丁显然是不可能合成的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2为0.4mol/L,O2为0.2mol/L | B. | SO2为0.15mol/L | ||
| C. | SO2,SO3均为0.25mol/L | D. | SO3为0.4mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com