
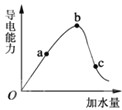
一定温度下,冰醋酸加水稀释过程中溶液的导电能力如图所示。请完成下列问题:

(1)“O”点为什么不导电?_________________。
(2)a、b、c三点pH由大到小的顺序为_______________________________________。
(3)a、b、c三点中醋酸的电离程度最大的点是_____________点。
(4)若使c点溶液中c(CH3COO-)提高,可以采取的措施有①__________,②____________, ③_____________,④_____________,⑤_____________。
(1)无水不电离,无自由移动的离子 (2)a>c>b
(3)c (4)Mg Na2O NaOH Na2CO3 CH3COONa
【解析】
试题分析:(1)CH3COOH是一种共价化合物,是弱电解质,共价化合物只有在水溶液里才能电离导电。“O”点不导电说明此时CH3COOH未电离,说明此时无水,不电离,不存在自由移动离子。
(2)pH大小取决于c(H+),pH越大,c(H+)越小,导电能力越弱;pH越小,c(H+)越大,导电能力越强。故pH大小顺序为a>c>b。
(3)电离度与溶液浓度有关,浓度越大,电离度越小,浓度越小,电离度越大,故c点电离度最大。
(4)欲使c(CH3COO-)增大,可以使平衡右移,即消耗c(H+)的办法,此时可考虑醋的五大通性中适合的有加金属、金属氧化物、碱、某些盐,也可以使平衡逆向移动,此时只能加醋酸盐。
考点:考查外界条件对醋酸电离平衡的影响、溶液导电性的判断以及氢离子浓度的大小比较等
点评:该题是中等难度的试题,试题基础性强,侧重考查学生分析问题、解决问题的能力。该题学生需要明确的是醋酸的电离程度增大,但溶液的导电性并不一定是增大,即溶液导电性只与溶液中离子浓度大小和离子所带电荷数有关系。


 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:
 在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示.请回答:
在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:
 如图所示,一定温度下,冰醋酸加水稀释过程中溶液的导电能力曲线图,请回答.
如图所示,一定温度下,冰醋酸加水稀释过程中溶液的导电能力曲线图,请回答.查看答案和解析>>
科目:高中化学 来源: 题型:
 在一定温度下,冰醋酸加水稀释过程中溶液的导电能力如图所示,请回答:
在一定温度下,冰醋酸加水稀释过程中溶液的导电能力如图所示,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:
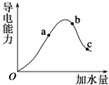 一定温度下,冰醋酸加水稀释过程中溶液的导电能力有如图所示曲线,请回答.
一定温度下,冰醋酸加水稀释过程中溶液的导电能力有如图所示曲线,请回答.| c(H+) | c(CH3COOH) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com