
【题目】下列各组化合物中,只含有离子键的是( )
A.NaOH和NaHSB.CaCl2和Na2O
C.CO2和K2SD.H2O2和HCl
科目:高中化学 来源: 题型:
【题目】某种有机化合物的结构简式如图所示。有关该物质的说法中正确的是
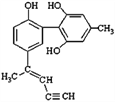
A. 该物质有四种官能团,其中一种名称为羟基
B. 1mol该物质H2反应时最多消耗H2 9mol
C. 滴入酸性KMnO4溶液振荡,紫色褪去,能证明其结构中存在碳碳双键
D. 该分子中的所有碳原子不可能共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:CH3—CH===CH2+HBr―→CH3—CHBr—CH3(主要产物),1 mol某烃A充分燃烧后可以得到8 mol CO2和4 mol H2O。该烃A在不同条件下能发生如下图所示的一系列变化。

(1)A的化学式:___________________,
(2)A的结构简式:_________________________。
(3)写出C、D、E、H物质的结构简式:
C____________________,D________________,E________________,H_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下用0.1000mol/L的盐酸分别逐滴加入到20.00mL0.1000mol/L的三种一元碱XOH、MOH、YOH溶液中,溶液的pH随加入盐酸体积的变化如图所示。下列叙述错误的是

A. XOH为强碱,MOH、YOH均为弱碱
B. V[HCl(aq)]=15.00mL时,三种溶液中离子总浓度大小顺序:XOH>MOH>YOH
C. V[HCl(aq)]=20.00mL时,三种溶液中水的电离程度:XOH>MOH>YOH
D. V[HCl(aq)]=40.00ml.时,YOH溶液中:c(H+)=c(Y+)+c(OH-)+2c(YOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:H2SO3![]() HSO3-+H+ Kal;HSO3-
HSO3-+H+ Kal;HSO3-![]() SO32-+H+ Ka2。25℃时,向某浓度的H2SO3溶液中逐滴滴加一定浓度的NaOH溶液,所得溶液中H2SO3、HSO3-、SO32-三种微粒的物质的量分数(δ)与溶液pH的关系如图所示。下列说法错误的是
SO32-+H+ Ka2。25℃时,向某浓度的H2SO3溶液中逐滴滴加一定浓度的NaOH溶液,所得溶液中H2SO3、HSO3-、SO32-三种微粒的物质的量分数(δ)与溶液pH的关系如图所示。下列说法错误的是
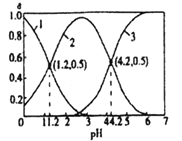
A. 曲线3表示的微粒是SO32-
B. 25℃时,Kal/ Ka2=1000
C. 溶液的pH=1.2时,溶液中有c(Na+)+c(H+)=c(OH-)+c(H2SO3)
D. 溶渡的Ph=4.2时,溶液中有c(Na+)+c(H+)=c(OH-)+2c(SO32-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是常温下,浓度为0.01mol/L的NaOH溶液与几种酸或盐混合后的情况:
混合组别 | 混合前酸或盐的总浓度 | 混合比例及混合溶液性质 |
① | c(HA)=0.02mol/L | 等体积混合,pH>7 |
② | HB溶液的pH=2 | V1mLNaOH溶液与V2mLHB溶液,pH=7 |
③ | c(H2C)=0.01mol/L | 等体积混合,pH>7 |
④ | c(NaHD)=0.01mol/L | 等体积混合,pH=7 |
回答下列问题:
(1)①组混合液中,HA、A-、Na+三种粒子浓度由大到小的顺序为________,若pH=8,则c(Na+)-c(A-)=________mol/L(填具体数字)。
(2)由②组混合液pH=7可推知,V1____V2。
(3)③组混合液中,pH>7的原因是______________________。
(4)0.01mol/LNaHD溶液中,水的电离度=_________。(已知:水的电离度=[已电离的水分子的个数/水分子总数]×100%)
(5)仅凭上述结果,一定能确定HA、HB、H2C、H2D四种酸中属于弱酸的是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】几种物质在酸性溶液中的还原性强弱顺序如下:SO2>I->Fe2+>H2O2。据此判断下列反应不能发生的是
A. 2Fe3++SO2+2H2O=2Fe2++SO![]() +4H+
+4H+
B. H2O2+H2SO4=SO2↑+O2↑+2H2O
C. SO2+I2+2H2O=H2SO4+2HI
D. 2Fe3++2I-=2Fe2++I2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式错误的是
A. 盐酸与烧碱溶液反应:H++OH-===H2O
B. 澄清石灰水中通入CO2变浑浊:CO2+Ca2++2OH-===CaCO3↓+H2O
C. 向氯化铝溶液中加入足量氨水:Al3++3OH-===Al(OH)3↓
D. Cl2与水反应生成盐酸和次氯酸:Cl2+H2O![]() H++Cl-+HClO
H++Cl-+HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】玻璃与人们的生产生活密切相关,玻璃制品随处可见。
(1)一般住宅的玻璃窗是普通玻璃,制造普通玻璃的主要原料是________、________、________,将原料粉碎后放入玻璃窑中在高温条件下发生反应即可制得玻璃,则普通玻璃的主要成分是________、________、________。
(2)某玻璃用三种氧化物的组合形式表示组成时,其中Na2O、CaO、SiO2的质量之比为31∶28∶180,则此玻璃的组成为________(填序号)。
A.Na2O·CaO·6H2SiO3
B.Na2O·CaO·6SiO2
C.2Na2O·2CaO·9SiO2
D.6Na2O·6CaO·SiO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com