
| ��+�� |
| 2 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����״���£�11.2 L H2O�������ķ�����Ϊ0.5 NA |
| B�������£�32 g O3��������ԭ����Ϊ2 NA |
| C��1 mol?L-1 NaOH��Һ������Na+������ΪNA |
| D��5.6 g Fe��2.24 L Cl2��ַ�Ӧ��ת�Ƶĵ�����Ϊ0.2 NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
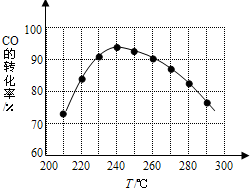 �����ѣ�CH3OCH3����δ������������ͺ�Һ������Ϊ�ྻҺ��ȼ��ʹ�ã���ҵ����CO��H2Ϊԭ������CH3OCH3�Ĺ�����Ҫ����������Ӧ��
�����ѣ�CH3OCH3����δ������������ͺ�Һ������Ϊ�ྻҺ��ȼ��ʹ�ã���ҵ����CO��H2Ϊԭ������CH3OCH3�Ĺ�����Ҫ����������Ӧ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �ŵ� |
| ��� |
| A���ŵ�ʱ���õ���ǽ���ѧ��ת��Ϊ���� |
| B�����ʱ��Rx+�������������ƶ� |
| C���ŵ�ʱ�����������ķ�ӦΪLi-e-�TLi+ |
| D�����ʱ�����������ķ�ӦΪR-xe-�TRx+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��c��OH-��/c��NH3?H2O�� |
| B��c��NH3?H2O��/c��OH-�� |
| C��c��H+����c��OH-���ij˻� |
| D��c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��0.1 mol?L-1 pHΪ4��NaHB��Һ�У�c��HB-����c��H2B����c��B2-�� |
| B�������ʵ���Ũ�ȵ�������Һ�У���NH4Al��SO4��2����NH4Cl����CH3COONH4�� ��NH3?H2O��c��NH4+�� �ɴ�С��˳���ǣ��٣��ڣ��ۣ��� |
| C��a mol?L-1HCN��Һ��b mol?L-1NaOH��Һ�������Ϻ�������Һ��c��Na+����c��CN-������aһ������b |
| D��0.1mol?L-1�Ĵ����pH=a��0.01mol?L-1�Ĵ����pH=b����a+1=b |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com