
�й����ʵ����ļ�����գ�
(1)2 mol CO(NH2)2�к�________mol C��________mol N��________mol H��������ԭ�Ӹ�________mol H2O������ԭ�Ӹ�����ȡ�
(2)�ٱ�״���£�22.4 L CH4����1.5 mol NH3����1.806��1024��H2O���ܱ�״���£�73 g HCl����Hԭ�Ӹ����ɶൽ�ٵ�˳����____________________��
(3)2.3 g Na�к�________mol e������������ˮ��Ӧ�в�����״ ���µ�H2________L��
���µ�H2________L��
(4)��0.4 mol Al2(SO4)3����Һ�У���________mol SO42����Al3�����ʵ���________0.8 mol(�>������<������)��
������(3)n(Na)��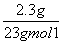 ��0.1 mol������1��Naԭ���к���11�����ӣ���2.3 g Na�к��е��ӵ����ʵ���n(e��)��11
��0.1 mol������1��Naԭ���к���11�����ӣ���2.3 g Na�к��е��ӵ����ʵ���n(e��)��11 n(Na)��1.1 mol
n(Na)��1.1 mol
2Na��2H2O===2NaOH��H2��
2 mol 22.4 L
0��1 mol x
x��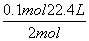 ��1.12 L
��1.12 L
(4)n(SO42��)��3n[Al2(SO4)3]��3��0.4 mol��1.2 mol��0.4 mol Al2(SO4)3�к���0.8 mol Al3������������Һ��Al3��ˮ�⣬��С��0.8 mol��
�𰸡�(1)2��4��8��2��(2)��>��>��>��
(3)1.1��1.12��(4)1.2��<


 ͬ����ϰ���ϴ�ѧ������ϵ�д�
ͬ����ϰ���ϴ�ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��B��C��D�dz����IJ�ͬ����Ķ�����Ԫ�أ����ǵ�ԭ��������������֪����ֻ��һ���ǽ���Ԫ�أ�CԪ��ԭ��������������DԪ��ԭ�ӵ�������������һ�룬BԪ��ԭ�ӵ�������������DԪ��ԭ�ӵ�������������2����E��FҲ�Ƕ�����Ԫ�أ�E��Dͬ���壬F��Aͬ���塣
(1)д��F2E2�ĵ���ʽ��____________________________________________��
�仯ѧ������Ϊ____________________��
( 2)����Ԫ���е�������ɵ�������ˮ�����������У��ܴٽ�ˮ���������M��________________________________________________________________
2)����Ԫ���е�������ɵ�������ˮ�����������У��ܴٽ�ˮ���������M��________________________________________________________________
(д��ѧʽ��дһ�����ɣ���ͬ)��������ˮ���������N��________��
25 ��ʱ��pH��a��M��Һ����ˮ�������H��Ũ����pH��a��N��Һ����ˮ�������H��Ũ��֮��Ϊ________��
(3)�ס��ҡ����ֱ���B��C��D����Ԫ����ۺ���������Σ��ס��Ҷ������������Ӧ���ұ���������ͬ����Ӧ�IJ��ﲻͬ���ش��������⣺
��������Һ�л����μӹ����ı���Һ�������з�����Ӧ�����ӷ���ʽΪ_______________________________ ___________________________________��
___________________________________��
�������Һ�л����μӹ����ı���Һ�����۲쵽��ʵ������Ϊ______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
1866�꿭��������˱��ĵ���˫�������ƽ�������νṹ�������˱��IJ������ʣ�������һЩ������δ����������ܽ���������ʵ��( )
A�����ļ�λ��ȡ����ֻ��һ�� B��������H2�����ӳɷ�Ӧ
C���屽û��ͬ���칹�� D���ڶ��屽ֻ��һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����й�˵������ȷ����(����)
A������ͨ����۵⻯����Һ�У���Һ�����������ԣ�Cl2>I2
D�����õ���ˮ���ձ�Ϊϡ����
C��������Ư�۳���������ˮ�Ĵ��������ߵ�����ԭ����ͬ
D����ɫ��ҺC�м���AgNO3��Һ��������ɫ�������ټ���ϡ���ᣬ��������ʧ������ɫ��ҺC��һ������Cl��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��NA��ʾ�����ӵ�������ֵ������������һ����ȷ���� (����)��
A����1 mol NaHSO4�����У�����������Ϊ2NA
B��1 mol C4H10�����й��ۼ�����Ϊ13NA
C��0.5 mol��L��1 Ba(NO3)2��Һ�У�NO3������ĿΪNA
D���κ������£�20 L N2���еķ�������������ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����100 mL 1 mol��L��1 NaCl��Һ�����в����д������ (����)��
A����������ƽ�Ϸ���Ƭ��Сһ����ֽ��Ȼ���Ȼ��Ʒ���ֽƬ�ϳ���
B���ѳƵõ��Ȼ��Ʒ���ʢ����������ˮ���ձ��У��ܽ⡢��ȴ���ٰ���Һ��������ƿ��
C��������ˮϴ���ձ�����������2��3�Σ�ϴ��ҺҲ��������ƿ��
D���ز�����������ƿ�м�������ˮ��ֱ����Һ��Һ��ǡ����̶�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��10.6 g Na2CO3����ˮ���1 L�� Һ
Һ
(1)����Һ��Na2CO3�����ʵ���Ũ��Ϊ________����Һ��Na�������ʵ���Ũ��Ϊ________��
(2)�����Һ�м���һ����NaCl���壬ʹ��Һ��Na�������ʵ���Ũ��Ϊ0.4 mol��L��1(������Һ�������)�����NaCl������Ϊ________��Cl�������ʵ���Ũ��Ϊ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵������ȷ����
A. ����ϩ�Ƴɵ����Ͽ��Է����������ڣ��������Բ���
B. ͨ���߷��ӻ�ѧ��Ӧ���ɺϳɴ����ض����ܻ��ŵ��µĸ߷��ӻ����
C. ���Ʊ�����ˮ����֬ʱҪ���뽻�������Եõ�������״�ṹ����֬
D. ͨ��˵������ϳɲ�����ָ���ϡ��ϳ���ά���ϳ�ϴ�Ӽ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
һ���¶��£���NaOH��Һ�м���һ�������ƿ飬��ַ�Ӧ��ָ���ԭ���¶ȣ�����˵����ȷ����(����)
A����Һ�������������ӣ��ܼ��������٣���Һ�����ʵ������������
B����Һ��pH���䣬�������ų�
C����Һ�е�Na����Ŀ��С���������ų�
D����Һ�е�c(Na��)�����������ų�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com