
���� ��1�������Ȼ�ѧ����ʽ��д����д������ע���ʾۼ�״̬�ͷ�Ӧ�ʱ䣻
��2�������Ȼ�ѧ����ʽ��˹���ɼ���õ��Ȼ�ѧ����ʽ���õ���Ӧ���ʱ䣻
��3����ȼ�����ɵ�����ˮ��
��4�����ݸ�˹���ɼ����ʱ䣬����д�Ȼ�ѧ����ʽ��
��� �⣺��1��0.4molҺ̬���������������ⷴӦ�����ɵ�����ˮ�������ų�256.65kJ��������32g��ȼ�շ���641.625kJ����ȼ�յ��Ȼ�ѧ����ʽΪ��N2H4��l��+2H2O2��l���TN2��g��+4H2O��g����H=-641.625kJ/mol��
�ʴ�Ϊ��N2H4��l��+2H2O2��l���TN2��g��+4H2O��g����H=-641.625kJ/mol��
��2����N2H4��l��+2H2O2��l���TN2��g��+4H2O��g����H=-641.625kJ/mol��
��H2O��l���TH2O��g����H=+44kJ/mol��
���ݸ�˹���ɣ���-�ڡ�4�õ���N2H4��l��+2H2O2��l���TN2��g��+4H2O��l����H=-817.625kJ/mol
��16gҺ̬��������Һ̬�������ⷴӦ���ɵ�����Һ̬ˮ����ʱ408.8KJ��
�ʴ�Ϊ��408.8KJ��
��3����ȼ�����ɵ�����ˮ�����ͷŴ����ȺͿ��ٲ������������⣬���ɵ���������Ⱦ��
�ʴ�Ϊ������N2��H2O���Ի�������Ⱦ��
��4����N2��g��+2O2��g���T2NO2��g����H=+67.7KJ•mol-1��
��N2H4��g��+O2��g���TN2��g��+2H2O ��g����H=-534KJ•mol-1
������ʽ2��-�ٵ�2N2H4��g��+2NO2��g��=3N2��g��+4H2O��g����H=2��-534KJ•mol-1��-��+67.7KJ•mol-1��=-1135.7kJ•mol-1��
�ʴ�Ϊ��2N2H4��g��+2 NO2 ��g���T3N2��g��+4 H2O��g����H=-1135.7kJ•mol-1��
���� ���⿼���˻�ѧ��Ӧ�����仯�ļ���Ӧ�ã����ʽṹ�����жϣ���˹���ɵļ��㣬�Ȼ�ѧ����ʽ��д��������Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 6.02��1023 | B�� | 1.204��1024 | C�� | 2 | D�� | 1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �����£���һ��4L���ܱ������г���5.2molH2��2molN2����Ӧ�����ж�NH3��Ũ�Ƚ��м�⣬�õ������������ʾ��
�����£���һ��4L���ܱ������г���5.2molH2��2molN2����Ӧ�����ж�NH3��Ũ�Ƚ��м�⣬�õ������������ʾ��| ʱ��/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c��NH3��/mol•L-1 | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
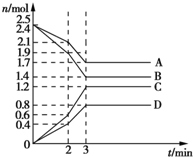 ��ij�ݻ�Ϊ2L���ܱ������У�A��B��C��D�����������ʷ������淴Ӧ�������ʵ���n��mol����ʱ��t��min���ı仯��ͼ��ʾ������˵����ȷ���ǣ�������
��ij�ݻ�Ϊ2L���ܱ������У�A��B��C��D�����������ʷ������淴Ӧ�������ʵ���n��mol����ʱ��t��min���ı仯��ͼ��ʾ������˵����ȷ���ǣ�������| A�� | ǰ2min�ڣ�v��A��=0.2 mol/��L•min�� | |
| B�� | ��2minʱ��ͼ�����ı��ԭ��ֻ����������ѹǿ | |
| C�� | �����������䣬3minʱ��ϵ��ѹǿ���ٷ����仯 | |
| D�� | ��������D��Ũ�ȣ�A�ķ�Ӧ������֮��С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
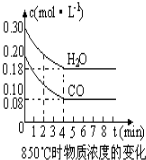 ��һ���Ϊ10L�������У�ͨ��һ������CO��H2O����850��ʱ�������·�Ӧ��CO��g��+H2O��g��?CO2��g��+H2 ��g����H��0��CO��H2OŨ�ȱ仯��ͼ��
��һ���Ϊ10L�������У�ͨ��һ������CO��H2O����850��ʱ�������·�Ӧ��CO��g��+H2O��g��?CO2��g��+H2 ��g����H��0��CO��H2OŨ�ȱ仯��ͼ��| ʱ�䣨min�� | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����Ȼ��� | B�� | Һ̬�Ȼ��� | C�� | �Ҵ���Һ | D�� | Һ̬�������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com