
| A. | 盐酸滴在石灰石上:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 少量CO2通入NaOH溶液中,:CO2+2OH-═CO32-+H2O | |
| C. | NaOH溶液和KHSO4溶液反应:OH-+H+═H2O | |
| D. | Na2O溶于稀盐酸:O2-+2H+═H2O |
分析 A.石灰石的主要成分为碳酸钙,碳酸钙与盐酸反应生成氯化钙、二氧化碳气体和水;
B.二氧化碳少量,反应生成碳酸钠和水;
C.氢氧化钠与硫酸氢钠的反应实质为氢离子与氢氧根离子反应生成水;
D.氧化钠为氧化物,离子方程式中氧化钠不能拆开.
解答 解:A.盐酸滴在石灰石上,碳酸钙需要保留化学式,反应的离子方程式为:CaCO3+2H+═Ca2++H2O+CO2↑,故A正确;
B.少量CO2通入NaOH溶液中,反应生成碳酸钠和水,反应的离子方程式为:CO2+2OH-═CO32-+H2O,故B正确;
C.NaOH溶液和KHSO4溶液反应,硫酸氢钾完全电离,二者反应的离子方程式为:OH-+H+═H2O,故C正确;
D.氧化钠溶于稀盐酸,氧化钠应该保留化学式,正确的离子方程式为:Na2O+2H+═H2O+2Na+,故D错误;
故选D.
点评 本题考查了离子方程式的书写判断,为中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法,如检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
 在一定的温度和容积为l L的密闭容器中投入A、B、C三种气态物质的浓度随时间的变化情况如图所示,下列结论中不正确的是( )
在一定的温度和容积为l L的密闭容器中投入A、B、C三种气态物质的浓度随时间的变化情况如图所示,下列结论中不正确的是( )| A. | t1时刻之后,若再加入一定量的A,达平衡时A的转化率降低 | |
| B. | t1时刻之后,3v(A)逆=2v(C)正 (v-速率) | |
| C. | t1时刻之后,若升高温度,混合气体的平均摩尔质量增大,则该反应A消耗的方向为吸热反应 | |
| D. | 在温度和容积固定不变的条件下,起始投入1molB、3molC达平衡时A的体积分数为3/7 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
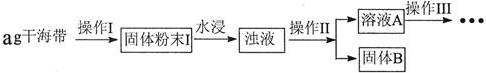
| 序号 | 实验方案 | 实验现象 | 结论 |
| ① | 取少量稀释后的溶液A加入淀粉后再用硫酸酸化,分装于试管Ⅰ、Ⅱ | 无现象 |  |
| ② | 往试管Ⅰ中加入FeCl2溶液后,加入2滴KSCN溶液并振荡 | 无现象 | 证明不是以IO3-形式存在 |
| ③ | 往试管Ⅱ中加入3%H2O2溶液并振荡 | 溶液变蓝 | 证明以I-形式存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度 实验 次数 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | 4.0℃ |
| 2 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 3 | 26.4 | 26.2 | 26.3 | 30.4 | |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Y的最高价氧化物的水化物具有弱酸性 | |
| B. | 阳离子的氧化性:Y>W | |
| C. | 原子半径:Z>Y | |
| D. | 元素W、X、Z各自最高和最低化合价的代数和分别为0、4、4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com