
分析 (1)①游离态是元素以单质的形式存在,化合态是元素在化合物中的形式存在,海水中镁元素以盐的形式存在;
②海水中含有大量的NaCl,而Na、K元素都以化合态形式存在;
(2)①正常雨水中溶解二氧化碳,其pH=5.6,故pH值小于5.6的雨水为酸雨;
②氟氯烃会破坏臭氧层.
解答 解:(1)①镁最外层电子数为2,易失去,易被氧化,性质活泼,在自然界中只能以化合物的形式存在,海水中镁元素以盐的形式存在,主要是化合态,
故答案为:化合态;
②海水中含有大量的NaCl,提取NaCl不需要经过化学变化,而Na、K元素都以化合态形式存在,由化合态转化为单质,一定需要经过化学变化,通常电解氯化钠固体得到金属钠,电解氯化钾固体得到金属钾,
故答案为:C;
(2)①正常雨水中溶解二氧化碳,饱和时其pH=5.6,酸雨是由化石燃料燃烧产生的二氧化硫、二氧化氮等酸性气体,二氧化硫与水反应生成亚硫酸,亚硫酸在空气中与氧气反应生成硫酸;二氧化氮与水等反应生成硝酸,故pH值小于5.6的雨水为酸雨,
故答案为:5.6;
②氮气、CO不会破坏臭氧层,氟氯烃会破坏臭氧层,
故答案为:C.
点评 本题考查海水资源开发利用、环境污染等,比较基础,注意对基础知识积累掌握,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 通入CO2,溶液pH减小 | |
| B. | 加入少量NH4Cl固体,平衡向正反应方向移动 | |
| C. | 慢慢升高温度,$\frac{c(HC{O}_{3}^{-})}{c(C{O}_{3}^{2-})}$逐渐减小 | |
| D. | 加入NaOH 固体后冷却到室温,溶液的KW=c(OH-)•c(H+)不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(Na+)=c(HA-)+2c(A2-)+c(OH-) | |
| B. | c(H2A)+c(HA-)+c(A2-)=0.1 mol•L-1 | |
| C. | 将上述溶液稀释至0.01 mol•L-1,c(H+)•c(OH-)不变 | |
| D. | 溶液中存在:c(Na+)>c(HA-)>c(OH-)>c(H2A)>c(H+)>c( A2-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②⑤ | B. | ②⑤⑥ | C. | ②④⑤⑥ | D. | ①②③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3可以用于治疗胃酸过多 | |
| B. | 浓硝酸具有强氧化性,因此浓硝酸可以作为漂白剂 | |
| C. | SiO2可以用于生产太阳能电池 | |
| D. | 在FeCl3饱和溶液里通入足量NH3可制取Fe(OH)3胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
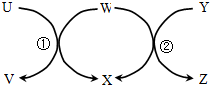 如图中U→Z六种物质在适当条件下能实现图示箭头方向一步转化,且反应①、②均为置换反应,满足条件的物质组是( )
如图中U→Z六种物质在适当条件下能实现图示箭头方向一步转化,且反应①、②均为置换反应,满足条件的物质组是( )| 序号 | U | W | Y | X |
| ① | Na | H2O | Na2O2 | NaOH |
| ② | Fe | H2O | C | H2 |
| ③ | HBr | Cl2 | CH4 | HCl |
| ④ | CuCl2(aq) | Al | HCl(aq) | AlCl3(aq) |
| A. | ②④ | B. | ②③ | C. | ①②④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硫能使织物褪色,对金属材料也有腐蚀作用 | |
| B. | 大量焚烧田间秸秆会污染空气 | |
| C. | 漂白粉在空气中能稳定存在,可用于漂白纸张 | |
| D. | PM2.5是指大气中直径小于或等于2.5微米(2.5×10-6m)的细小可吸入颗粒物,其分散在空气中可能形成胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4LCl2与足量NaOH溶液反应转移的电子数为NA | |
| B. | 25℃,0.1mol•L-1的NaOH溶液中含有OH-的数目为0.1NA | |
| C. | 标准状况下,11.2L乙醇中含有的氢原子数为3NA | |
| D. | 标况下,7.8g苯中含有碳碳双键的数目为0.3NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com