
| A. | ①④ | B. | ①③④ | C. | ②③ | D. | ②④ |
分析 ①工业用氨气催化氧化生成一氧化氮,一氧化氮氧化生成二氧化氮,二氧化氮与水反应生成硝酸;
②工业上常以食盐为原料制备氯气,氯气通入石灰乳制备漂白粉;
③工业上制Mg的过程:将MgC12溶液经蒸发结晶得到MgC12•6H2O,然后MgC12•6H2O在一定条件下加热得到无水MgC12,最后电解熔融的氯化镁可得到Mg;
④从铝土矿中提取铝反应过程 ①溶解:将铝土矿溶于NaOH(aq):Al₂O₃+2NaOH=2NaAlO+H₂O ②过滤:除去残渣氧化亚铁(FeO)、硅铝酸钠等 ③酸化:向滤液中通入过量CO2,NaAlO2+CO₂+2H₂O=Al(OH)₃↓+NaHCO₃④过滤、灼烧 Al(OH)₃得到氧化铝,⑤电解熔融的氧化铝生成铝.
解答 解:①工业用氨气催化氧化生成一氧化氮,一氧化氮氧化生成二氧化氮,二氧化氮与水反应生成硝酸,过程为:NH3 $\stackrel{O_{2}}{→}$ NO $\stackrel{H_{2}O、O_{2}}{→}$HNO3,故正确;
②工业上制备漂白粉的工业流程:①NaCl溶液$\stackrel{通电}{→}$Cl2 $\stackrel{石灰乳}{→}$ 漂白粉,故错误;
③工业上制Mg的工业流程:MgC12溶液:MgCl2(aq)$\stackrel{蒸发结晶}{→}$MgC12•6H2O$\stackrel{HCl}{→}$无水MgCl2 $\stackrel{电解}{→}$ Mg
,故错误;
④工业制铝流程:铝土矿 $\stackrel{NaOH溶液}{→}$ NaAlO2溶液 $\stackrel{过量CO_{2}酸化}{→}$ Al(OH)3$\stackrel{灼烧}{→}$ Al2O3$\stackrel{电解}{→}$ Al,故正确;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,涉及工业制备物质的流程,熟悉反应原理是解题关键,注意相关知识的积累,题目难度中等.


 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案科目:高中化学 来源: 题型:选择题
| A. | SO2和SiO2 | B. | CCl4和KCl | C. | NaOH和CaCl2 | D. | CO2和H2S |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.0g H218O与T2O的混合物中所含中子数 | |
| B. | 250mL 1mol/LFeCl3溶液中,阴、阳离子总数 | |
| C. | 标准状况下,7g某单烯烃A中的C-H键数 | |
| D. | 200mL 10mol/L盐酸与足量MnO2反应,转移电子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
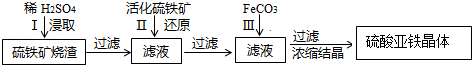
| pH | 开始沉淀 | 沉淀完全 |
| Fe(OH)2 | 5.8 | 8.8 |
| Fe(OH)3 | 1.1 | 3.2 |
| Al(OH)3 | 3.0 | 5.0 |
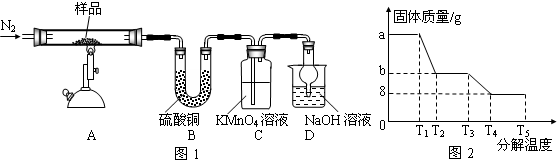
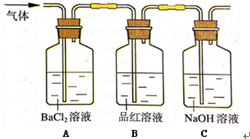 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
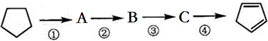
| A. | A的结构简式是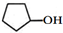 | |
| B. | ①②的反应类型分别是取代、消去 | |
| C. | 反应②③的条件分别是浓硫酸加热、光照 | |
| D. | 酸性KMnO4溶液褪色可证明 已完全转化 已完全转化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
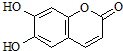
| A. | 与稀H2SO4混合加热不反应 | |
| B. | 不能使酸性高锰酸钾溶液褪色 | |
| C. | 1mol 瑞香素最多能与3mol Br2发生反应 | |
| D. | 1mol瑞香素与足量的NaOH溶液发生反应时,消耗NaOH 3mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Y和Z可以组成一种Y和Z的质量比为7:20的共价化合物 | |
| B. | X,Y、Z可以组成一种盐,其中X、Y、Z元素原子个数比为4:2:3 | |
| C. | Y和W组成的化合物与X和Z组成的化合物反应可生成2种碱性物质 | |
| D. | 由X、Y、Z三种元素中的任意两种组成的具有10电子的微粒有2种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com