
| A. | 将铝片插入硝酸铜溶液中:Cu2++Al=Al3++Cu | |
| B. | 盐酸与饱和的澄清石灰水反应:H++OH-══H2O | |
| C. | 碳酸钙与醋酸反应:CaCO3+2H+══Ca2++CO2↑+H2O | |
| D. | 稀硫酸滴在铜片上:Cu+2H+═Cu2++H2↑ |
分析 A.根据电荷守恒判断,该离子方程式两边正电荷不相等;
B.稀盐酸和氢氧化钙反应生成氯化钙和水,澄清石灰水写离子;
C.碳酸钙与醋酸反应生成醋酸钙、水、二氧化碳,碳酸钙、醋酸、水、二氧化碳在离子反应中保留化学式;
D.铜不活泼,与稀硫酸不反应.
解答 解:A.铝片插入硝酸铜溶液中,反应生成铝离子和铜,离子方程式必须满足电荷守恒,正确的离子方程式为:3Cu2++2Al=2Al3++3Cu,故A错误;
B.稀盐酸和氢氧化钙反应生成氯化钙和水,澄清石灰水写离子,离子方程式为:H++OH-═H2O,故B正确;
C.碳酸钙与醋酸反应生成醋酸钙、水、二氧化碳,碳酸钙、醋酸、水、二氧化碳在离子反应中保留化学式,离子反应为CaCO3+2CH3COOH=2CH3COO-+Ca2++CO2↑+H2O,故C错误;
D.铜与稀硫酸不反应,故D错误;
故选B.
点评 本题考查离子方程式正误判断,明确离子方程式书写规则及物质性质即可解答,检验方法有:检查反应能否发生,检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

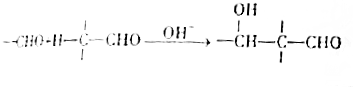
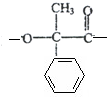
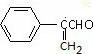 +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$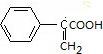 +Cu2O+2H2O
+Cu2O+2H2O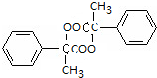
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知:0.4mol液态N2H4与足量的液体双氧水反应,生成氮气和水蒸气,放出200.0kJ的热量.
已知:0.4mol液态N2H4与足量的液体双氧水反应,生成氮气和水蒸气,放出200.0kJ的热量.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
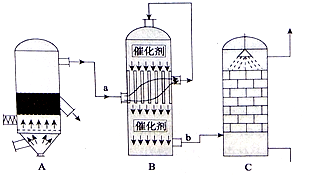
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、K+、Cl-、HCO3- | B. | K+、Ba2+、OH-、NO3- | ||
| C. | Mg2+、Cu2+、Cl-、SO42- | D. | Na+、Cl-、Ba2+、SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用酚酞试纸 | B. | 用湿润的蓝色石蕊试纸 | ||
| C. | 用硝酸银溶液 | D. | 用湿润的淀粉-KI试纸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com