

分析 (1)①根据题中所示的石灰乳的作用是吸收尾气二氧化硫来回答;
②根据实验的操作原则,为了让气体尽可能转化,要根据反应所需的条件和用量严格操作;
③考虑氮气的化学性质稳定,空气中氧气的活泼性等因素的影响;
(2)制取的原理是碳酸根和锰离子之间反应生成碳酸锰的过程,但要考虑MnCO3难溶于水、乙醇并在潮湿时易被空气氧化,100℃开始分解以及Mn(OH)2开始沉淀时pH=7.7等因素,过程中控制溶液的PH值以及洗涤沉淀所选的溶剂要小心,据此答题.
解答 解:(1)①石灰乳的作用是吸收尾气二氧化硫,碱和酸性氧化物反应得到对应的盐和水,反应方程式为SO2+Ca(OH)2=CaSO3+H2O,
故答案为:SO2+Ca(OH)2=CaSO3+H2O;
②为使SO2尽可能转化完全,应定要保证控制反应的温度,在通入SO2和N2比例一定、不改变固液投料的条件下,要求所通气体一定要慢,
故答案为:控制适当的温度、缓慢通入混合气体;
③氮气的化学性质稳定,空气中氧气性质活泼,在Mn2+催化作用下,易把亚硫酸氧化成硫酸,而使硫酸根浓度增大,
故答案为:Mn2+催化O2与H2SO3反应生成H2SO4(或H2SO3+O2=H2SO4);
(2)制取的原理是碳酸根和锰离子之间反应生成碳酸锰的过程,但要考虑MnCO3难溶于水、乙醇并在潮湿时易被空气氧化,100℃开始分解以及Mn(OH)2开始沉淀时pH=7.7等因素,过程中控制溶液的PH值以及洗涤沉淀所选的溶剂要小心,所以实验步骤为)①边搅拌边加入 Na2CO3,并控制溶液pH<7.7;②过滤,用少量水洗涤2~3次;③检验SO42-是否被洗涤干净:取最后一次洗涤液于试管中,滴加BaCl2溶液,再滴加稀盐酸,若无沉淀生成,则洗涤干净;④用少量C2H5OH洗涤;⑤低于100℃干燥,
故答案为:①Na2CO3;pH<7.7;②过滤,用少量水洗涤2~3次;③取最后一次洗涤液于试管中,滴加BaCl2溶液,再滴加稀盐酸,若无沉淀生成,则洗涤干净;⑤低于100℃干燥.
点评 本题主要考查了制备高纯碳酸锰实验方案,读懂工艺流程,正确识图、理解离子反应的本质是解答的关键,本题实验综合性强,难度中等.


科目:高中化学 来源: 题型:解答题
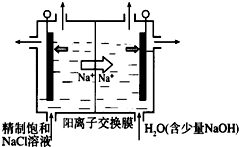 二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.
二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
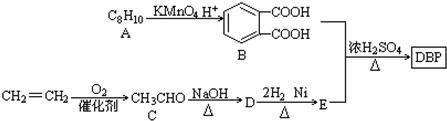
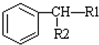 $\stackrel{KMnO_{2}H+}{→}$
$\stackrel{KMnO_{2}H+}{→}$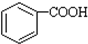
 (-R1、-R2表示氢原子或烃基)
(-R1、-R2表示氢原子或烃基)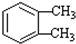 ,D→E的反应类型加成(或还原)反应.
,D→E的反应类型加成(或还原)反应.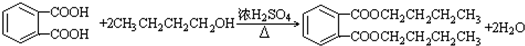 .
.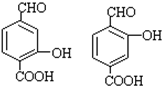 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(Na+)=1mol/L,c(Cl-)=1mol/L,c(Ca2+)=2mol/L,c(ClO4-)=4mol/L | |
| B. | c(K+)=1mol/L,c(Mg2+)=1mol/L,c(Cu2+)=1mol/L,c(NO${\;}_{3}^{-}$)=4mol/L | |
| C. | c(OH-)=1mol/L,c(SO${\;}_{4}^{2-}$)=1mol/L,c(NH${\;}_{4}^{+}$)=6mol/L,c(HCO${\;}_{3}^{-}$)=1mol/L | |
| D. | c(Al3+)=1mol/L,c(SO${\;}_{4}^{2-}$)=1mol/L,c(OH-)=2mol/L,c(Na+)=2mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加热灼烧海带时要在蒸发皿中进行 | |
| B. | 蒸馏时,水从冷凝管上部通入,从下部流出 | |
| C. | 向某溶液中加入AgNO3溶液,生成白色沉淀,该溶液一定含有Cl- | |
| D. | 分液时,碘的四氯化碳溶液从分液漏斗下口放出,水层从上口倒出 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K2FeO4是新型水处理剂,其原理与明矾相同 | |
| B. | Fe2O3俗称铁红,常用作红色油漆和涂料 | |
| C. | 推广应用燃料“脱硫、脱硝”技术,可减少硫氧化物和氮氧化物对空气的污染 | |
| D. | Al2O3熔点高,可用于制作耐高温仪器 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
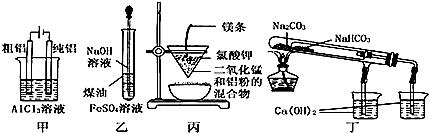
| A. | 用甲图装置电解精炼铝 | |
| B. | 用乙图装置制备 Fe(OH)2 | |
| C. | 用丙图装置可制得金属锰 | |
| D. | 用丁图装置验证 NaHCO3 和 Na2CO3的热稳定性 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com