
| A. | X、Y相对分子质量之差为84 | |
| B. | X中含有HCOO-,Y中含有-OH | |
| C. | Y的分子式为:C7H8O3 | |
| D. | 若X中有四种氢,则满足条件的X可能有两种 |
分析 1molX水解得到1molY和2mol醋酸,则X为酯,Y中含有羟基,且Y分子中至少含有2个O原子,Y分子中C、H两种元素总质量分数为65.2%,1-65.2%=34.8%,通过讨论判断X的分子量,然后得出C、H的总原子量,再利用商余法得出Y的分子式;
A.1molX水解得到1molY和2mol醋酸,结合酯的水解原理判断X、Y相对分子质量之差;
B.根据Y的分子式及其具有的化学性质判断其含有的官能团类型;
C.根据分析判断Y的分子式;
D.根据信息可知,X分子中含有1个-CHO和2个-OOCCH3,若X有4种H,则X具有对称结构,1个-CHO和-OOCCH3有2种H原子,苯环上含有2种H,据此写出其可能的结构简式.
解答 解:1molX水解得到1molY和2mol醋酸,则X为酯,Y中含有羟基,且Y分子中至少含有2个O原子,
Y分子中C、H两种元素总质量分数为65.2%,1-65.2%=34.8%,
当含有2个O原子时,Y的相对分子质量为:$\frac{16×2}{34.8%}$≈92<100不符合;
当含有3个O原子时,Y的相对原子质量为:$\frac{16×3}{34.8%}$≈138,不符合;
当含有4个O原子时,Y的相对原子质量为:$\frac{16×4}{34.8%}$≈183>150,不符合,
所以Y的相对分子质量为138,Y分子中含有C、H的总原子量为:138-16×3=90,
根据商余法可知:$\frac{90}{14}$=6…6>2,所以Y分子中应该含有7个C,含有H原子数为:$\frac{90-12×7}{1}$=6,
所以Y的分子式为:C7H6O3,
A.1molX与2mol水发生水解反应得到1molY和2mol醋酸,则X、Y相对分子质量之差=2个醋酸的分子量-2个水的分子量=84,故A正确;
B.X溶液能发生银镜反应,则X中含有醛基,根据分析可知,X中含有2个羟基,其含有3个O原子,则X分子中应该还含有1个醛基,不会含有HOOC-结构,故B错误;
C.根据分析可知,Y的分子式为C7H6O3,故C错误;
D.根据分析可知,X分子中含有1个-CHO和2个-OOCCH3,若X有4种H,则X具有对称结构,1个-CHO和-OOCCH3有2种H原子,苯环上含有2种H,X的可能结构有: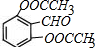 、
、 ,总共有2种结构,故D正确;
,总共有2种结构,故D正确;
故选AD.
点评 本题考查了有机物分子式、结构简式的确定,题目难度中等,明确常见有机物结构与性质为解答关键,注意掌握质量守恒定律在确定有机物分子式中的应用方法,试题培养了学生的分析能力及化学计算能力.


 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | 摩尔是一个物理量,是6.02×1023个粒子、 | |
| B. | 摩尔是物质质量的单位 | |
| C. | 摩尔是表示物质的量的单位 | |
| D. | 摩尔的标准是0.12kg12C中所含有的原子数目 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 编号 | I | II | III |
| 实验 |  |  |  |
| 现象 | 有白色沉淀生成,滤液为蓝色 | 有白色沉淀生成,滴加稀硝酸,沉淀不溶解 | |
| 化学方程式 | 2AgNO3+CuCl2═2AgCl↓+Cu(NO3)2 | ||
| 离子方程式 | Ba2++SO42-═BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 溶液一定显碱性 | B. | 溶液不可能显碱性 | ||
| C. | 溶液可能显碱性 | D. | 溶液不可能显酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | NaHCO3和Na2O2 | B. | 铝粉和NaOH | C. | Na2SO3和SO3 | D. | Na2CO3和P2O5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④⑥⑦ | B. | ①②③⑥ | C. | ①③④⑤⑦ | D. | ③④⑤⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com