
| A. | 单质:⑥⑦ | B. | 氧化物:②⑨ | C. | 碱:①④ | D. | 有机物:③⑤ |
分析 液氧、水银等物质都是由一种元素组成的纯净物,属于单质;
生石灰、干冰、等物质都是由氧元素和另外一种元素组成的化合物,属于氧化物;
烧碱电离时生成的阴离子都是氢氧根离子,属于碱;
甲烷、酒精等物质都是含有碳元素的化合物,属于有机物;
纯碱、碳酸氢铵等物质属于盐.
解答 解:A、干冰是二氧化碳的固体,属于氧化物,不属于单质.故A错误;
B、水银是汞,是由汞元素组成的纯净物,属于单质,不属于氧化物.故B错误;
C、纯碱是由钠离子和碳酸根离子组成的化合物,属于盐,不属于碱.故C错误;
D、甲烷、酒精等物质都是含有碳元素的化合物,属于有机物.故D正确.
故选D.
点评 本题主要考查物质的分类方法,解答时要分析物质的元素组成,然后再根据各类物质概念的含义进行分析、判断;特别要注意纯碱虽然是含有碳元素的化合物,但是性质与无机物相似,属于无机物.


 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 用含少量铁的氧化物的氧化铜制取氯化铜晶体(CuCl2•xH2O).有如图操作:
用含少量铁的氧化物的氧化铜制取氯化铜晶体(CuCl2•xH2O).有如图操作:查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向沸水中滴加少量饱和氯化铁溶液,加热至溶液呈红褐色,用激光笔照射 | 有丁达尔效应 | 红褐色液体为胶体 |
| B | 向溶液X中加入NaHCO3粉末 | 产生无色气体 | X一定属于酸 |
| C | 向淀粉NaI溶液中加入氯水 | 溶液变蓝 | 氧化性:Cl2>I2 |
| D | 将气体X分别通入溴水和酸性高锰酸钾溶液 | 两溶液均褪色 | X可能是SO2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.3 mol•L-1•s-1 | B. | 0.4 mol•L-1•s-1 | C. | 0.6 mol•L-1•s-1 | D. | 0.8 mol•L-1•s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,2.24L水所含的分子数目为0.1 NA | |
| B. | 9g水中含有的电子数目为0.5NA | |
| C. | 0.3 mol/L的MgCl2溶液中含Mg2+数目为0.3 NA | |
| D. | 常常压下,28gN2和CO混合气体中所含有的原子数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
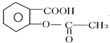 具有的官能团有酯基和羧基(写名称).用阿司匹林和氢氧化钠中和制得可溶性阿司匹林,该反应的化学方程式为C6H5OOCCH3COOH+H2O→CH3COOH+C6H5OHCOOH.
具有的官能团有酯基和羧基(写名称).用阿司匹林和氢氧化钠中和制得可溶性阿司匹林,该反应的化学方程式为C6H5OOCCH3COOH+H2O→CH3COOH+C6H5OHCOOH.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com