
二氧化氯(ClO2)是一种高效、广谱、安全的杀菌消毒剂。
(1)氯化钠电解法是一种可靠的工业生产ClO2的方法。
①用于电解的食盐水需先除去其中的Ca2+、Mg2+、SO 等杂质。除杂操作时,往粗盐水中先加入过量的________(填化学式),至沉淀不再产生后,再加入过量的Na2CO3和NaOH,充分反应后将沉淀一并滤去。经检测发现滤液中仍含有一定量的SO
等杂质。除杂操作时,往粗盐水中先加入过量的________(填化学式),至沉淀不再产生后,再加入过量的Na2CO3和NaOH,充分反应后将沉淀一并滤去。经检测发现滤液中仍含有一定量的SO ,其原因是________________________________________________________________________。
,其原因是________________________________________________________________________。
[已知:Ksp(BaSO4)=1.1×10-10,Ksp(BaCO3)=5.1×10-9]
②该法工艺原理如下图。其过程是将食盐水在特定条件下电解得到的氯酸钠(NaClO3)与盐酸反应生成ClO2。

工艺中可以利用的单质有________(填化学式),发生器中生成ClO2的化学方程式为________________________________________________________________________。
(2)纤维素还原法制ClO2是一种新方法,其原理是:纤维素水解得到的最终产物D与NaClO3反应生成ClO2。完成反应的化学方程式:
 __(D)__+24NaClO3+12H2SO4===
__(D)__+24NaClO3+12H2SO4=== ClO2↑+
ClO2↑+ CO2↑+18H2O+
CO2↑+18H2O+ ________
________
(3)ClO2和Cl2均能将电镀废水中的CN-氧化为无毒的物质,自身被还原为Cl-。处理含CN-相同量的电镀废水,所需Cl2的物质的量是ClO2的________倍。
答案 (1)①BaCl2 BaSO4和BaCO3的Ksp相差不大,当溶液中存在大量CO 时,BaSO4(s)会部分转化为BaCO3(s)(或其他合理答案)
时,BaSO4(s)会部分转化为BaCO3(s)(或其他合理答案)
②H2、Cl2 2NaClO3+4HCl===2ClO2↑+Cl2↑+2NaCl+2H2O
(2)1C6H12O6+24NaClO3+12H2SO4===24ClO2↑+6CO2↑+18H2O+12Na2SO4
(3)2.5
解析 (1)①根据Ksp相差不大,沉淀转化不彻底来回答。
②根据工艺原理可以判断,在氯化钠电解槽中生成NaClO3和H2,在ClO2发生器中除生成ClO2外,还有Cl2产生,所以可以利用的单质有H2、Cl2。生成ClO2的化学方程式为2NaClO3+4HCl===2ClO2↑+Cl2↑+2NaCl+2H2O。
(2)纤维素最终水解生成葡萄糖(C6H12O6),根据原子守恒可以判断最后一种产物为Na2SO4。
(3)1 mol Cl2得2 mol电子,而1 mol ClO2得5 mol电子,所以处理相同物质的量的CN-,所需Cl2的物质的量是ClO2的2.5倍。


 华东师大版一课一练系列答案
华东师大版一课一练系列答案 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:高中化学 来源: 题型:
铁是人类应用较早,当前应用量最大的金属元素。下列有关铁及其化合物的有关说法中正确的是( )
A.赤铁矿的主要成分是Fe3O4
B.铁与水蒸气在高温下的反应产物为Fe2O3和H2
C.除去FeCl2溶液中的FeCl3杂质可以向溶液中加入铁粉,然后过滤
D.Fe3+与KSCN产生血红色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述错误的是( )
A.只用水就可以鉴别四氯化碳、苯和乙醇
B.CCl4可由CH4制得,可萃取碘水中的碘
C.石油和天然气的主要成分都是碳氢化合物
D.苯不能使酸性高锰酸钾溶液褪色,因此苯不能发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)____HCl(浓)+____MnO2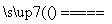 ____Cl2↑+____MnCl2+____H2O
____Cl2↑+____MnCl2+____H2O
(2)____Cu+____HNO3(稀)===____Cu(NO3)2+____NO↑+____H2O
(3)____KI+____KIO3+____H2SO4===____I2+____K2SO4+____H2O
(4)____MnO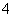 +____H++____Cl-===____Mn2++____Cl2↑+____H2O
+____H++____Cl-===____Mn2++____Cl2↑+____H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
在P+CuSO4+H2O—→Cu3P+H3PO4+H2SO4(未配平)的反应中,7.5 mol CuSO4可氧化P的物质的量为________mol。生成1 mol Cu3P时,参加反应的P的物质的量为________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图所示。
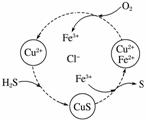
(1)在图示的转化中,化合价不变的元素是________。
(2)反应中当有1 mol H2S转化为硫单质时,保持溶液中Fe3+的物质的量不变,需消耗O2的物质的量为______。
(3)在温度一定和不补加溶液的条件下,缓慢通入混合气体,并充分搅拌。欲使生成的硫单质中不含CuS,可采取的措施有____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
配平下列方程式
(1)[2011·福建理综,23(6)]在某强酸性混合稀土溶液中加入H2O2,调节pH≈3,Ce3+通过下列反应形成Ce(OH)4沉淀得以分离。完成反应的离子方程式:
Ce3++H2O2+H2O===Ce(OH)4↓+________
(2)[2010·福建理综,24(2)改编]完成“氧化除铁”步骤中反应的离子方程式:
 Fe(OH)2+
Fe(OH)2+ ClO-+
ClO-+ ________===
________===
 Fe(OH)3+
Fe(OH)3+ Cl-
Cl-
(3)[2011·安徽理综,27(2)改编]配平反应的离子方程式:
 Mn2++
Mn2++ ClO
ClO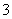 +
+ H2O===
H2O=== MnO2↓+
MnO2↓+ Cl2↑+
Cl2↑+ ________。
________。
(4)[2010·重庆理综,26(3)]配平用钙线脱氧脱磷的化学方程式:
 P+
P+ FeO+
FeO+ CaO
CaO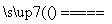
 Ca3(PO4)2+
Ca3(PO4)2+ Fe
Fe
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室用KClO3和浓盐酸反应也可以制备氯气。某研究性学习小组利用如图所示装置在实验室中制取Cl2并探究其相关性质:
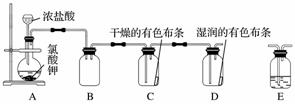
(1)装置A中存在一处错误,请改正这处错误:________________________。
(2)写出装置A中发生反应的化学方程式:________________________________________________________________________
________________________________________________________________________。
(3)为了除去氯气中的氯化氢,需要在装置A、B之间添加装置E,装置E中所盛装的试剂为________________。为了探究使有色布条褪色的是氯气还是氯气与水反应的生成物,需要在整套装置中添加装置E,其中加入浓硫酸,装置E在整套装置中的添加位置为________(填字母)。
a.A、B之间 b.B、C之间
c.C、D之间 d.D之后
(4)取下集气瓶B,将铁丝加热至红热状态,伸入集气瓶B中,可以观察到的现象是______________________,能检验该反应产物中铁元素价态的试剂是________(填字母)。
a.氯水 b.蒸馏水和铁粉
c.氢氧化钠溶液 d.KSCN溶液
(5)另外一个化学学习小组就环境保护方面指出了上述装置的缺陷,并给出了改进措施,该改进措施是________________________________________________________________________
__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
用惰性电极电解饱和Na2SO4溶液,一段时间后,析出w g Na2SO4·10 H2O晶体,阴极上放出a g气体,则饱和Na2SO4溶液的质量分数为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com