
工业上用铝土矿(主要成分为Al2O3,含有Fe2O3、SiO2等杂质)制取无水氯化铝的一种工艺流程示意如下:

已知:
物质 | SiCl4 | AlCl3 | FeCl3 | FeCl2 | NaCl |
沸点/℃ | 57.6 | 180(升华) | 300(升华) | 1023 | 801 |
回答下列问题:
(1)高温反应前,常在800℃焙烧铝土矿,使固体中水分挥发、气孔数目增多,其作用是 ___(只要求写出一种)。
(2)高温反应后,铝土矿中的氧化物均转变为相应的氯化物,由Al2O3、C和Cl2反应生成AlCl3的化学方程式为 。
(3)气体II的主要成分除了Cl2外,还含有 。气体II常用过量冷的NaOH溶液吸收,吸收液中含有的阴离子主要有 。
(4)工业上为了降低生产成本,生产过程中需要控制加入铝粉的量,“废渣”的主要成分是 。
(5)AlCl3和NaCl的熔融盐常用于镀铝电解池,电镀时AlCl-4和Al2Cl-7两种离子在电极上相互转化,其它离子不参与电极反应,电镀时阴极的电极反应式为 。
科目:高中化学 来源:2015-2016学年辽宁省高二下期中化学试卷(解析版) 题型:选择题
下列说法正确的是
A.按系统命名法,化合物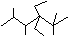 的名称是2,3,5,5-四甲基-4,4-二乙基己烷
的名称是2,3,5,5-四甲基-4,4-二乙基己烷
B.等物质的量的苯和苯甲酸完全燃烧消耗氧气的量不相等
C.苯和甲苯互为同系物,均能使KMnO4酸性溶液褪色
D.结构片段 的高聚物,其单体是苯酚和甲醛
的高聚物,其单体是苯酚和甲醛
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二下期中化学试卷(解析版) 题型:选择题
下列各有机物的名称错误的是
A.3-甲基-2-戊烯 B.2,2—二甲基丙烷 C.3-甲基-1-丁烯 D.3-甲基-2-丁烯
查看答案和解析>>
科目:高中化学 来源:2016届吉林省吉林市高三第三次调研理综化学试卷(解析版) 题型:填空题
【化学——选修3:物质结构与性质】
已知X、Y、Z、R、Q为周期表中原子序数依次增大的前36号元素。相关信息如下:
X元素是宇宙中最丰富的元素 |
Y元素基态原子的核外p电子数比s电子数少1 |
Z元素被誉为“太空金属”,也有“生物金属”之称,其基态原子次外层有2个未成对电子 |
R元素在元素周期表的第十一列 |
Q元素在周期表里与R元素在同一个分区 |
请回答下列问题:
(1)YX3中心原子的杂化轨道类型是 ,离子化合物YX5的电子式是 。
(2)CO与Y2属于等电子体,1 个CO分子中含有的π键数目是 个。
(3)工业上利用ZO2和碳酸钡在熔融状态下制取化合物A(A可看做
一种含氧酸盐)。A晶体的晶胞为正方体(如右图)。
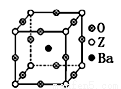
①制备A的化学反应方程式是 ;
②在A晶体中,Z的配位数为 ;
③在A晶体中,若将Z元素置于立方体的体心,Ba元素置于立方体的顶点,则O元素处于立方体的 。
(4)R2+离子的外围电子层电子排布式为 。R2O的熔点比R2S的 (填“高”或“低”)。
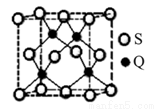
(5)Q元素和硫(S)元素能够形成化合物B。B晶体的晶胞为正方体(如右图),若晶胞棱长为540.0 pm,则晶胞密度为 g·cm—3(列式并计算)。
查看答案和解析>>
科目:高中化学 来源:2016届吉林省吉林市高三第三次调研理综化学试卷(解析版) 题型:选择题
镁电池放电时电压高而平稳,镁电池成为人们研制的绿色电池,一种镁电池的反应式为
xMg+Mo3S4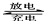 MgxMo3S4,下列说法中正确的是
MgxMo3S4,下列说法中正确的是
A.充电时MgxMo3S4只发生还原反应
B.放电时Mo3S4只发生氧化反应
C.充电时阳极反应式为 Mo3S42x-—2xe-= Mo3S4
D.放电时负极反应式为xMg= xMg2+—2xe-
查看答案和解析>>
科目:高中化学 来源:2016届四川省雅安市三诊理综化学试卷(解析版) 题型:选择题
常温下,有体积相同的四种溶液:①pH=2的CH3COOH溶液;②pH=2的硫酸;③pH=12的氨水;④pH=12的NaOH溶液。下列说法正确的是
A.①和②混合后:c(H+)=c(CH3COO-)+c(OH-)+2c(SO42-)
B.①和④溶液中:c(Na+)=c(CH3COO-)+c(CH3COOH)=0.01mol·L-1
C.②和③混合溶液中:c(SO42-)>c(NH4+ )>c(OH-)>c(H+)
D.四种溶液各稀释100倍,溶液的pH:④>③>①>②
查看答案和解析>>
科目:高中化学 来源:2016届四川省邛崃市高三强化训练一化学试卷(解析版) 题型:填空题
已知聚酯F是分子主链上带有苯环和酯基的特种工程塑料结构为
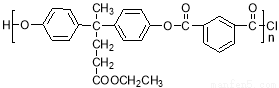
在航空航天等领域具有广泛应用。下图是利用乙酰丙酸CH3COCH2CH2COOH,合成聚酯F的路线如下:

已知:①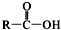 +SOCl2→
+SOCl2→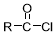 +SO2+HCl ②
+SO2+HCl ② +R′OH→
+R′OH→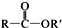 +HCl(R、R′表示烃基)
+HCl(R、R′表示烃基)
(1)乙酰丙酸中含有的官能团是羰基和_______________(填官能团名称)
(2)C的系统命名为____________________
(3)B、E合成聚酯F的反应类型为_______________________________
写出D生成E的化学反应方程式_________________________________________________
(4)乙酰丙酸生成A的化学反应方程式为___________________________________________
(5)下列关于有机物B的说法正确的是_______________(填字母代号)。
a.1mol该物质最多能与2molNaOH反应b.1mol该物质最多能与2molBr2发生取代反应
c.不能发生消去反应 d.能与H2发生加成反应
(6)符合下列条件的D的同分异构体有_______________种。
①能发生银镜反应 ②能与NaHCO3溶液反应 ③分子中有苯环,分子中无 结构
结构
查看答案和解析>>
科目:高中化学 来源:2016届天津市河东区高三第二次模拟考试理综化学试卷(解析版) 题型:选择题
下列说法正确的是
A.反应A(g) ? 2B(g) △H,若正反应的活化能为Ea kJ/mol,逆反应的活化能为Eb kJ/mol,则△H=-( Ea- Eb)kJ/mol
B.常温下,pH相同的NaOH溶液和Ba(OH)2溶液中,水的电离程度相同
C.某温度氯化钠在水中的溶解度是20 g,该温度饱和氯化钠溶液的质量分数为20%
D.将浓度为0.1 mol/L HF溶液加水不断稀释过程中,电离平衡常数Ka(HF)保持不变,始终保持增大
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三5月模拟一理综化学试卷(解析版) 题型:实验题
某小组以CoCl2·6H2O、NH4Cl、H2O2、液氨、氯化铵为原料,在活性炭催化下合成了橙黄色晶体X。为测定其组成,进行如下实验。
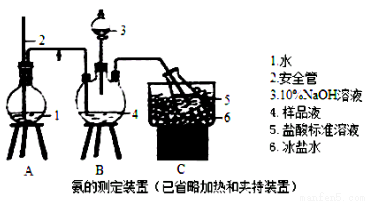
①氨的测定:精确称取wgX,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10% NaOH溶液,通入水蒸气,将样品溶液中的氨全部蒸出,用V1 mL c1 mol·L-1的盐酸溶液吸收。蒸氨结束后取下接收瓶,用c2 mol·L-1 NaOH标准溶液滴定过剩的HCl,到终点时消耗V2mL NaOH溶液。
②氯的测定:准确称取样品X,配成溶液后用AgNO3标准溶液滴定,K2CrO4溶液为指示剂,至出现砖红色沉淀不再消失为终点(Ag2CrO4为砖红色)。
回答下列问题::
(1)装置中安全管的作用原理是 。
(2)用NaOH标准溶液滴定过剩的HCl时,应使用 式滴定管,可使用的指示剂为 。
(3)样品中氨的质量分数表达式为 。
(4)测定氨前应该对装置进行气密性检验,若气密性不好测定结果将 (填“偏高”或“偏低”)。
(5)测定氯的过程中,使用棕色滴定管的原因是 ;滴定终点时,若溶液中c(Ag+)=2.0×10-5mol·L-1,c(CrO42-)为 mol·L-1。(已知:Ksp(Ag2CrO4)=1.12×10-12)
(6)经测定,样品X中钴.氨.氯的物质的量之比为1:6:3,钴的化合价为 ,制备X的化学方程式为 ;X的制备过程中温度不能过高的原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com