
(12分)A、B、C、D是原子序数依次增大的短周期主族元素,A、C在元素周期表中的相对位置如图,A元素最外层与次外层上的电子数之差为3,B为地壳中含最最多的金属元素。
(1)D离子结构示意图为_____________。
(2)将C的低价态氧化物甲通入到D单质的水溶液会使之褪色,写出该反应的离子方程 式_______________。
(3)A的最高价氧化物对应的水化物是乙,现将过量Cu加入到100 mL 8.0 mol/L乙的浓溶液中,充分 反应,共收集到6.72L(标准状况)气体,则该气体的成分是_________,还原剂失电子数为_________________。
(4)将两份足量的B单质分别加入到等体积等浓度的盐酸和NaOH溶液中,充分反应生成气体的体积比为_________,若将反应后所得的溶液混合,会生成白色沉淀,发生反应的离子方程式为_________________;B单质表面的氧化膜可用NaOH溶液除去,写出该反应的化学方程式____________________ _。
26.(1) (1分 ) (2) SO2+Cl2+2H2O=SO42-+2Cl-+4H+ (2分)
(1分 ) (2) SO2+Cl2+2H2O=SO42-+2Cl-+4H+ (2分)
(3)NO和NO2 (2分) 3.01×1023 (2分)
(4)1∶3 (1分);Al3++3AlO2-+6H2O=4Al(OH)3↓(2分)Al2O3+2NaOH=2NaAlO2+H2O (2分)。
【解析】
试题分析:根据题意可知:A是N,B是Al,C是S;D是Cl. (1)D离子结构示意图为 ;(2)将C的低价态氧化物甲SO2通入到D单质Cl2的水溶液会发生氧化还原反应,使之褪色,该反应的离子方程式是SO2+Cl2+2H2O=SO42-+2Cl-+4H+;(3)A的最高价氧化物对应的水化物是乙HNO3,若将过量Cu加入到100 mL 8.0 mol/L乙的浓溶液中,首先发生反应:Cu+4HNO3(浓)=Cu(NO3)2+NO2↑+2H2O,产生NO2,当反应进行到一定程度后硝酸变为稀硝酸,会发生反应:3Cu+8HNO3(稀)=2Cu(NO3)2+2NO↑+4H2O,充分反应,共收集到6.72L(标准状况)气体,则该气体的成分是NO和NO2;还原剂失电子的物质的量等于硝酸铜中结合的NO3-的物质的量,为0.1L×8.0 mol/L-(6.72L÷22.4L/mol)=0.5mol,所以n(e-)=0.5mo ×6.02×1023/mol=3.01×1023; (4)将两份足量的B单质分别加入到等体积等浓度的盐酸和NaOH溶液中,根据反应方程式:2Al+6HCl=2AlCl3+3H2↑;2Al+2NaOH+2H2O=2NaAlO2+3H2↑可知充分反应生成气体的体积比为1∶3,若将反应后所得的溶液混合,会生成白色沉淀,发生反应的离子方程式为Al3++3AlO2-+6H2O=4Al(OH)3↓;在B单质表面的氧化膜Al2O3是两性氧化物,既可以与酸反应,也可与碱发生反应,可用NaOH溶液除去,该反应的化学方程式是Al2O3+2NaOH=2NaAlO2+H2O 。
;(2)将C的低价态氧化物甲SO2通入到D单质Cl2的水溶液会发生氧化还原反应,使之褪色,该反应的离子方程式是SO2+Cl2+2H2O=SO42-+2Cl-+4H+;(3)A的最高价氧化物对应的水化物是乙HNO3,若将过量Cu加入到100 mL 8.0 mol/L乙的浓溶液中,首先发生反应:Cu+4HNO3(浓)=Cu(NO3)2+NO2↑+2H2O,产生NO2,当反应进行到一定程度后硝酸变为稀硝酸,会发生反应:3Cu+8HNO3(稀)=2Cu(NO3)2+2NO↑+4H2O,充分反应,共收集到6.72L(标准状况)气体,则该气体的成分是NO和NO2;还原剂失电子的物质的量等于硝酸铜中结合的NO3-的物质的量,为0.1L×8.0 mol/L-(6.72L÷22.4L/mol)=0.5mol,所以n(e-)=0.5mo ×6.02×1023/mol=3.01×1023; (4)将两份足量的B单质分别加入到等体积等浓度的盐酸和NaOH溶液中,根据反应方程式:2Al+6HCl=2AlCl3+3H2↑;2Al+2NaOH+2H2O=2NaAlO2+3H2↑可知充分反应生成气体的体积比为1∶3,若将反应后所得的溶液混合,会生成白色沉淀,发生反应的离子方程式为Al3++3AlO2-+6H2O=4Al(OH)3↓;在B单质表面的氧化膜Al2O3是两性氧化物,既可以与酸反应,也可与碱发生反应,可用NaOH溶液除去,该反应的化学方程式是Al2O3+2NaOH=2NaAlO2+H2O 。
考点:考查元素的推断、化学方程式的书写、计算的知识。


科目:高中化学 来源:2015届山东省高三上学期第二次月考联考化学试卷(解析版) 题型:选择题
已知反应:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O,据此判断下列说法正确的是
A.反应生成物都属于电解质 B.HCl全部发生氧化反应
C.该反应表明氧化性KClO3比Cl2强 D.1mol KClO3在反应中得到6mole-
查看答案和解析>>
科目:高中化学 来源:2015届山东省菏泽市高三上学期期中联考化学试卷(A)(解析版) 题型:选择题
下列说法正确的是
A.某物质经科学测定只含有一种元素,则可以断定该物质是一种纯净物
B.不能用瓷坩埚加热熔融氢氧化钠固体
C.将SO2通入品红溶液或溴水均能使它们褪色,证明SO2有漂白性
D.向某溶液中滴加氯水后,滴加KSCN溶液,溶液变红,证明溶液中含有Fe2+
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三上学期第一次质量检测化学试卷(解析版) 题型:选择题
如图为含有同一种元素的a、b、c、d、e五种物质的转化关系。
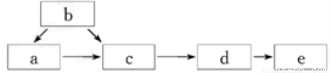
其中a是单质,b是气态氢化物,c、d是氧化物,e是该元素最高价氧化物对应的水化物,则a可能是( )
①C ②N2 ③S ④F2
A.只有①和③ B.只有④ C.①②③ D.①②③④
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三上学期第一次质量检测化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A、我国自主研发的“龙芯1号”CPU芯片与光导纤维是同种材料
B、需要通过化学反应才能从海水中获得食盐和淡水
C、水晶项链和餐桌上的瓷盘都是硅酸盐制品
D、粗硅制备单晶硅涉及氧化还原反应
查看答案和解析>>
科目:高中化学 来源:2015届山东省聊城市高三上学期第一次阶段性测试化学试卷(解析版) 题型:选择题
将4.6 g Cu和Mg完全溶于浓硝酸溶液中,反应中硝酸的还原产物为4480mL NO2气和336 mL N2O4气体(标准状况下),反应后的溶液中,加入过量NaOH溶液,生成沉淀的质量为 ( )
A.9.02 g B.8.51 g C.8.26 g D.7.04 g
查看答案和解析>>
科目:高中化学 来源:2015届山东省聊城市高三上学期第一次阶段性测试化学试卷(解析版) 题型:选择题
下列各组反应最终有白色沉淀生成的是( )
①金属钠投入到FeCl2溶液中 ②过量NaOH溶液和AlCl3溶液混合
③少量Ca(OH)2投入NaHCO3溶液中 ④过量CO2通入NaAlO2溶液中
A.②③ B.③④ C.①③④ D.①②③④
查看答案和解析>>
科目:高中化学 来源:2015届山东省烟台市高三上学期期中考试化学试卷(解析版) 题型:填空题
(7分)实验证明,以下六种物质是一个氧化还原反应的反应物和生成物:NO、FeSO4、H2O、Fe(NO3)3、HNO3和Fe2(SO4)3。
(1)这六种物质中,反应物是____________;被还原的元素是____________。
(2)若该反应是恰好完全反应,且收集到NO的体积为4.48L(标况时),测得反应后溶液的体积为250mL。
反应过程中转移的电子数为___________;所得溶液中SO42-的物质的量浓度为________mol·L-1。
查看答案和解析>>
科目:高中化学 来源:2015届山东省潍坊市诸城高三10月月考化学试卷(解析版) 题型:实验题
(6分)溶液配制是中学化学实验的基本操作。
(1)用氢氧化钠固体配制100g10%的氢氧化钠溶液时,需要用到的玻璃仪器有玻璃棒和 __________。
(2)配制一定物质的量浓度溶液时用到的仪器较多,下列有关叙述正确的是_____。
a.称量NaOH固体时,分别在天平的两个托盘垫上相同大小的纸片
b.玻璃棒的作用是搅拌、引流
c.用浓硫酸配制稀溶液时,在量筒中稀释后要冷却至室温再转移到容量瓶中
d.容量瓶在使用前要检查是否漏水
(3)实验室配制一定物质的量浓度溶液,试叙述定容操作的具体方法:向容量瓶中注入蒸馏水至离刻度线1~2cm处,然后________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com