
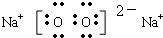 或 Na+[:H]-(2分)
或 Na+[:H]-(2分)

 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源:不详 题型:填空题
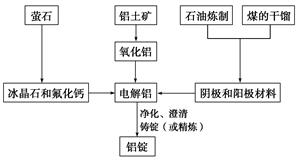
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.该物质是Al(OH)3和Na2CO3的混合物 |
| B.1 mol NaAl(OH)2CO3最多可消耗4 mol H+ |
| C.该药剂遇胃酸不产生气体,适合胃溃疡患者服用 |
| D.该物质属于两性氢氧化物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.只有② | B.①③ | C.②④ | D.②③ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
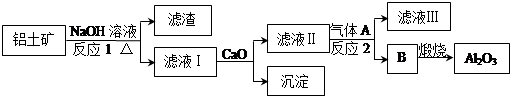
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.导致易拉罐变瘪的反应是:CO2 + 2OH- = CO32- + H2O |
| B.导致易拉罐又鼓起来的反应是:2Al + 2OH- + 2H2O = 2AlO2- + 3H2↑ |
| C.反应结束后,溶液中的离子浓度关系是:c(Na+) + c(H+) = c(OH-) +c(AlO2-) + c(CO32-) |
| D.如果将CO2换为NH3,浓NaOH溶液换为浓盐酸,易拉罐也会出现先瘪后鼓的现象 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
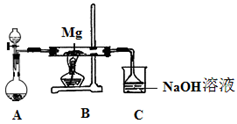
 2MgSO3+S;丙同学的推测是:3Mg+SO2
2MgSO3+S;丙同学的推测是:3Mg+SO2 2MgO+MgS,要验证甲、乙、丙三位同学的推测是否正确,丁同学作如下实验探究:
2MgO+MgS,要验证甲、乙、丙三位同学的推测是否正确,丁同学作如下实验探究:| 序号 | 实验步骤 | 预期现象和结论 |
| ① | 取少量反应后所得固体于试管中 | |
| ② | 向试管中的固体慢慢滴加 , 试管口塞上带导管的单孔塞,并将导管通入盛有 的试管中。 | 若试管中的 , 则丙同学推测正确。 若试管中的固体未完全溶解,且 ,则乙同学推测正确。 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
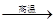 3Ba↑+BaO·Al2O3
3Ba↑+BaO·Al2O3查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
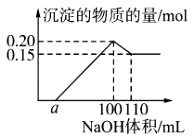
| A.该未知溶液中至少含有3种阳离子 |
| B.滴加的NaOH溶液的物质的量浓度为5 mol·L-1 |
| C.若另一种离子为二价阳离子,则a=10 |
| D.若将最终沉淀过滤、洗涤、灼烧,其质量一定为6 g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com