
 2C(g)£¬5minŗóø÷ČŻĘ÷·“Ó¦“ļĘ½ŗāדĢ¬,ĘäÖŠ¼×ČŻĘ÷ÖŠAµÄĪļÖŹµÄĮæĪŖ0.4mol”£
2C(g)£¬5minŗóø÷ČŻĘ÷·“Ó¦“ļĘ½ŗāדĢ¬,ĘäÖŠ¼×ČŻĘ÷ÖŠAµÄĪļÖŹµÄĮæĪŖ0.4mol”£| | ·“Ó¦Ē°ø÷ĪļÖŹµÄĪļÖŹµÄĮæ/mol | ||
| A | B | C | |
| ¼× | 1 | 3 | 0 |
| ŅŅ | 0 | 0 | 2 |
| ±ū | 1.5 | 4.5 | 1 |


 Č«ÓŲāŹŌ¾ķĻµĮŠ“š°ø
Č«ÓŲāŹŌ¾ķĻµĮŠ“š°ø ³å“Ģ100·Ö1ŗžķĻµĮŠ“š°ø
³å“Ģ100·Ö1ŗžķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā

| ŹµŃéŠņŗÅ | ĀČ»ÆĆ¾¹ĢĢåÖŠĀČŌŖĖŲŗ¬Įæ/% | ĪĀ¶Č/”ę | ·ŪĖé·½Ź½/ | “߻Ɗ§¹ū/g”¤g-1 |
| 1 | 70.97 | 20 | ¹ö¶ÆĒņÄ„ | 3.9”Į104 |
| 2 | 74.45 | 20 | ¹ö¶ÆĒņÄ„ | 5.0”Į104 |
| 3 | 74.45 | 20 | Õń¶ÆĒņÄ„ | 5.9”Į104 |
| 4 | ¦Ų | 100 | Õń¶ÆĒņÄ„ | |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
 N2 + 3H2£¬ŌŚÄ³ĪĀ¶ČĻĀµÄĘ½ŗā³£ŹżĪŖ0.25£¬ÄĒĆ“£¬ŌŚ“ĖĢõ¼žĻĀ£¬°±µÄŗĻ³É·“Ó¦1/2 N2 + 3/2 H2
N2 + 3H2£¬ŌŚÄ³ĪĀ¶ČĻĀµÄĘ½ŗā³£ŹżĪŖ0.25£¬ÄĒĆ“£¬ŌŚ“ĖĢõ¼žĻĀ£¬°±µÄŗĻ³É·“Ó¦1/2 N2 + 3/2 H2 NH3µÄĘ½ŗā³£ŹżĪŖ
NH3µÄĘ½ŗā³£ŹżĪŖ| A£®4 | B£®2 ”” | C£®1 | D£®0.5 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ŌŚĀČ»ÆīÜČÜŅŗÖŠ¼ÓČėŅ»¶ØĮæµÄÅØŃĪĖį£¬ČÜŅŗŃÕÉ«µÄ±ä»ÆŹĒÓÉ·ŪŗģÉ«±äĪŖĄ¶É« |
B£®ŅŃÖŖI3£ I2 + I££¬ĻņŹ¢ÓŠKI3ČÜŅŗµÄŹŌ¹ÜÖŠ¼ÓČėŹŹĮæCCl4£¬Õńµ“¾²ÖĆŗóCCl4²ćĻŌ×ĻŗģÉ«£¬ĖµĆ÷KI3ŌŚCCl4ÖŠµÄČܽā¶Č±ČŌŚĖ®ÖŠµÄ“ó I2 + I££¬ĻņŹ¢ÓŠKI3ČÜŅŗµÄŹŌ¹ÜÖŠ¼ÓČėŹŹĮæCCl4£¬Õńµ“¾²ÖĆŗóCCl4²ćĻŌ×ĻŗģÉ«£¬ĖµĆ÷KI3ŌŚCCl4ÖŠµÄČܽā¶Č±ČŌŚĖ®ÖŠµÄ“ó |
| C£®ŌŚ”°¶ĘŠæĢśĘ¤µÄ¶Ę²ćŗń¶ČµÄ²ā¶Ø”±ŹµŃéÖŠ£¬½«¶ĘŠæĢśĘ¤·ÅČėĻ”ĮņĖį£¬“ż²śÉśĒāĘųµÄĖŁĀŹĶ»Č»¼õŠ”£¬æÉŅŌÅŠ¶ĻŠæ¶Ę²ćŅŃ·“Ó¦ĶźČ« |
| D£®±ź¶ØNaOHČÜŅŗµÄ»ł×¼ĪļÖŹæÉÓĆ²ŻĖį”¢±½¼×Ėį”¢ĮŚ±½¶ž¼×ĖįĒā¼Ų |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
 CO£Øg£©£«3H2£Øg£©£»”÷H£½£«206 kJ/mol£¬Ņ»¶ØĢõ¼žĻĀĻņĢå»żĪŖ1 LµÄĆܱÕČŻĘ÷ÖŠ³äČė1 mol CH4ŗĶ1 mol H2O£¬²āµĆCH4£Øg£©ŗĶCO£Øg£©µÄÅضČĖꏱ¼ä±ä»ÆĒśĻßČēĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ £Ø £©
CO£Øg£©£«3H2£Øg£©£»”÷H£½£«206 kJ/mol£¬Ņ»¶ØĢõ¼žĻĀĻņĢå»żĪŖ1 LµÄĆܱÕČŻĘ÷ÖŠ³äČė1 mol CH4ŗĶ1 mol H2O£¬²āµĆCH4£Øg£©ŗĶCO£Øg£©µÄÅضČĖꏱ¼ä±ä»ÆĒśĻßČēĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ £Ø £©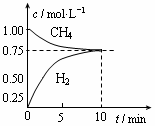
| A£®10minŹ±ÓĆCH4±ķŹ¾µÄ·“Ó¦ĖŁĀŹĪŖ0.075 mol?L£1?min£1 |
| B£®Ź¹ÓĆøߊ§“߻ƼĮÄܹ»Ōö“óCOµÄ²śĀŹ |
| C£®øĆĢõ¼žĻĀ·“Ó¦µÄĘ½ŗā³£ŹżĪŖ0.1875 |
D£®ÉżøßĪĀ¶ČÄÜŹ¹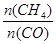 Ōö“ó Ōö“ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
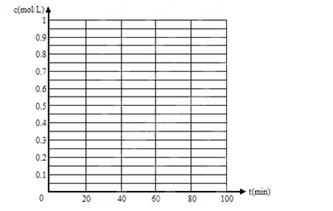
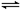 CO2(g)£«H2(g)£¬·“Ó¦ĪļCOµÄĪļÖŹµÄĮæŌŚ²»Ķ¬ĪĀ¶ČŹ±ĪļÖŹµÄĮæĖꏱ¼äµÄ±ä»ÆČēĻĀ±ķĖłŹ¾£¬»Ų“šĻĀĮŠĪŹĢā£ŗ
CO2(g)£«H2(g)£¬·“Ó¦ĪļCOµÄĪļÖŹµÄĮæŌŚ²»Ķ¬ĪĀ¶ČŹ±ĪļÖŹµÄĮæĖꏱ¼äµÄ±ä»ÆČēĻĀ±ķĖłŹ¾£¬»Ų“šĻĀĮŠĪŹĢā£ŗ| | 0min | 10min | 20min | 30min | 40min | 50min |
| 830”ę | 1mol | 0.8mol | 0.65mol | 0.55mol | 0.5mol | 0.5mol |
| 1100”ę | 1mol | 0.75mol | 0.6mol | 0.6mol | 0.6mol | 0.6mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
 2SO3£¬×“Ģ¬¢ņŹ±“ļĘ½ŗā£¬ŌņO2µÄ×Ŗ»ÆĀŹĪŖ£Ø £©
2SO3£¬×“Ģ¬¢ņŹ±“ļĘ½ŗā£¬ŌņO2µÄ×Ŗ»ÆĀŹĪŖ£Ø £©
| A£®40£„ | B£®60£„ | C£®80£„ | D£®90£„ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Ź³ĪļŌŚ³£ĪĀĻĀøÆ°ÜŹĒ×Ō·¢½ųŠŠµÄ | B£®·²ŹĒ·ÅČČ·“Ó¦¶¼ŹĒ×Ō·¢µÄ |
| C£®×Ō·¢·“Ó¦¶¼ŹĒģŲŌö“óµÄ·“Ó¦ | D£®µē½ā³ŲµÄ·“Ó¦ŹĒŹōÓŚ×Ō·¢·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
| A£®ĻąµČ”” | B£®Ē°Õߊ”ÓŚŗóÕß | C£®Ē°Õß“óÓŚŗóÕß | D£®ĪŽ·ØČ·¶Ø |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com