
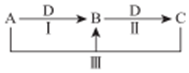
 A、B、C、D 都是中学化学中常见物质,其中 A、B、C 均含有同一种元素,在一定条件下相互转化关系如图(部分反应中的水已略去).
A、B、C、D 都是中学化学中常见物质,其中 A、B、C 均含有同一种元素,在一定条件下相互转化关系如图(部分反应中的水已略去).分析 (1)若A为氯碱工业的产品,C为厨房中的用品,可知A为NaOH,C为NaHCO3,A、B、C 均含有同一种元素,根据转化关系可知,B为Na2CO3,D为CO2,Na2CO3,NaHCO3是弱酸强碱盐,是在水的作用下而发生水解显碱性;
(2)D元素的一种红棕色氧化物常用作颜料,应为氧化铁,若A、D均为单质,且A为气体,则D为Fe,A为Cl2,B为FeCl3,C为FeCl2.
解答 解:(1)若A为氯碱工业的产品,C为厨房中的用品,可知A为NaOH,C为NaHCO3,B为Na2CO3,D为CO2,Na2CO3,
①反应Ⅲ为NaOH和NaHCO3的反应,反应的离子方程式是HCO3-+OH-=CO32-+H2O,
故答案为:HCO3-+OH-═CO32-+H2O;
②氯碱工业制氢氧化钠,是电解饱和食盐水,反应的化学方程式是2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑,
故答案为:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑;
(2)D元素的一种红棕色氧化物常用作颜料,应为氧化铁,则D为Fe,A为Cl2,B为FeCl3,C为FeCl2,
①反应Ⅲ为铁与铁离子反应生成亚铁离子,反应的离子方程式是Fe+2Fe3+═3Fe2+,
故答案为:Fe+2Fe3+═3Fe2+;
②B为FeCl3,氯化铁能净水是因为铁离子水解生成具有吸附性的Fe(OH)3,水解方程式为Fe3++3H2O?Fe(OH)3+3H+,由于酸性废水中的酸,会抑制铁离子的水解,所以不能使酸性废水中的悬浮物沉降除去,
故答案为:酸性废水中的酸,会抑制铁离子的水解.
点评 本题是以常见的化学物质为载体,考查了元素化合物质之间的转化及他们涉及的化学反应原是的相关知识,为高考常见题型,侧重于学生的分析能力、推断能力和综合运用元素化合物知识,注意把握题给信息,找出推断的突破口,把握相关物质的性质以及离子方程式、化学方程式的书写,难度中等.


 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 相同条件下,N2和O3的混合气体与等体积的N2所含原子数相等 | |
| B. | 标准状况下,28 g CO和22.4 L H2O所含分子数相等 | |
| C. | 5.6 g铁粉与足量盐酸充分反应,有0.2 mol电子转移 | |
| D. | 等质量的CH4和NH3所含电子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2和O2反应生成水 | B. | 锌片投入稀硫酸中 | ||
| C. | 木炭在高温下与CO2反应生成CO | D. | 2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
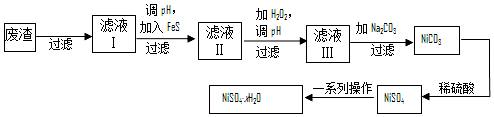
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
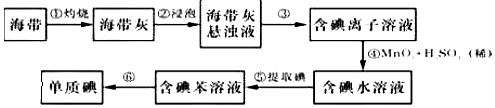
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
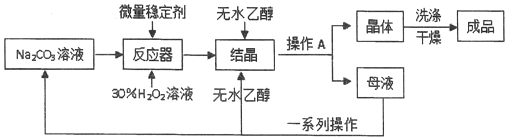
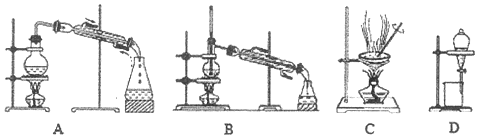

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol•L-1 CH3COOH溶液与0.1 mol•L-1NaOH溶液等体积混合 | |
| B. | 向40mL0.2 mol•L-1的NaOH溶液中通入67.2mLCO2(标况) | |
| C. | 在100mL1 mol•L-1NH4Cl溶液中,投入3.9gNa2O2 | |
| D. | 在20mL0.01 mol•L-1Ma(HCO3)2溶液中,投入0.2g Ma(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
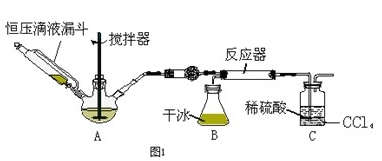
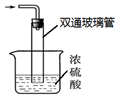
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸发溶剂 | B. | 升高温度 | C. | 降低温度 | D. | 加入KN03固体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com