
【题目】下列有关电池的叙述正确的是( )
A.锌锰干电池工作一段时间后碳棒变细
B.氢氧燃料电池工作时氢气在负极被氧化
C.太阳能电池的主要材料是高纯度的二氧化硅
D.氢氧燃料电池可将热能直接转变为电能
科目:高中化学 来源: 题型:
【题目】在密闭容器里,A与B反应生成C,其反应速率分别用v(A)、v(B)、v(C)表示,已知3v(B)=2v(A)、2v(C)=3v(B),则此反应可表示为
A.2A+3B = 2C B.A+3B = 2C C.3A+2B = 3C D.A+B = C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应2SO2(g)+O2(g)2SO3(g),能增大正反应速率的措施是( )
A.通入大量O2 B.增大容器容积 C.移去部分SO3 D.降低体系温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂。与Cl2相比, ClO2不但具有更显著的杀菌能力, 而且不会产生对人体有潜在危害的有机氯代物。
(1)在ClO2 的制备方法中, 有下列两种常用制备方法:
方法一:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
方法二:2NaClO3+H2O2+H2SO4=2ClO2↑+O2↑+Na2SO4+2H2O
①方法一中氧化剂与还原剂的物质的量之比为__________________,其中方法二制备的ClO2 更适合用于饮用水的消毒, 其主要原因是 。
(2)我国最近成功研制出制取ClO2 的新方法, 其反应的微观过程如图甲所示:
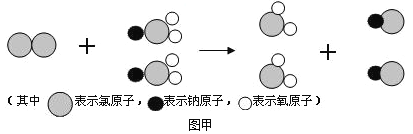
该反应的化学方程式为 。
(3)消毒时, ClO2对污水中Fe2+、Mn2+、S2-和CN— 等有明显的去除效果.某工厂污水中含CN—,现用ClO2将CN—氧化,生成两种无毒气体,其离子反应方程式为 。
(4)自来水厂用ClO2 处理后的水中, 要求ClO2 的浓度在0. 1~0. 8mg/L之间。碘量法可以检测水中ClO2 的浓度,步骤如下:
Ⅰ. 取一定体积的水样用氢氧化钠溶液调至中性, 然后加入一定量的碘化钾, 并加入淀粉溶液, 溶液变蓝。
Ⅱ. 加入一定量的Na2S2O3 溶液。(已知: 2S2O32- +I2 =S4O62- +2I - )
Ⅲ. 重复上述操作2~3次。
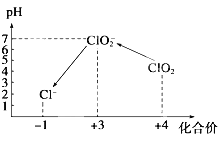
操作时, 不同pH环境中粒子种类如上图所示:
请回答:
①操作Ⅰ中反应的离子方程式是 ;
②确定操作Ⅱ恰好完全反应的现象是 ;
③若水样的体积为1. 0 L, 在操作Ⅱ时消耗了1. 0×10 -3 mol/L的Na 2 S 2 O 3 溶液10 mL, 则水样中ClO2 的浓度是 mg/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是
A. 分子式为C7H8O含有苯环且属于醇类的同分异构体有4种
B. 乙炔能使溴的四氯化碳溶液褪色是发生了氧化反应
C. 苯分子中所有原子都在同一平面上
D. 乙酸乙酯少量乙酸杂质可加饱和NaOH溶液后经分液除去
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学在人类生活中扮演重要角色,下列说法正确的是
A. 蔬菜和粗粮中富含纤维素,纤维素在人体中酶的作用下能水解成葡萄糖
B. 混凝法、中和法、沉淀法、氧化还原法是工业处理废水常用的方法
C. 可只用淀粉溶液检验食盐中是否加碘
D. 鸡蛋清溶液中加人饱和Na2SO4溶液,有沉淀生成是因为蛋白质变性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属及其化合物在生产中用途广泛。
Ⅰ.从含铜丰富的自然资源黄铜矿(CuFeS2)冶练铜的工艺流程如下:
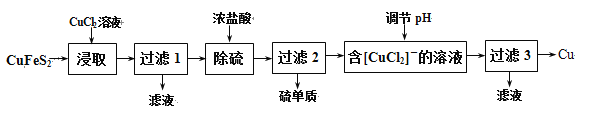
已知:CuFeS2+3CuCl2=4CuCl↓+FeCl2+2S↓
(1)浸取时,若改用FeCl3溶液,也能生成CuCl和S,该反应化学方程式为 。
(2)若过滤1所得滤液中只含FeCl2,则将其在空气中加热蒸干、灼烧后,所得固体的化学式为 。
(3)调节溶液的pH后,除生成Cu外,还能产生一种金属离子,此金属离子是 。(填离子符号)
(4)过滤3所得滤液中可以循环使用的物质有 ,为保持流程持续循环,每生成1molCu,理论上需补充CuCl2的物质的量为 。
Ⅱ.利用生产硼砂的废渣——硼镁泥(主要成分为MgCO3、SiO2,还含有少量Fe2O3、MnO、CaO等)为主要原料制取轻质碳酸镁[MgCO3·Mg(OH)2·2H2O]的工业流程如下:
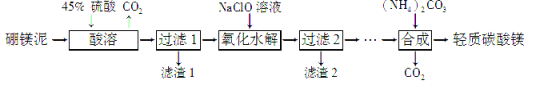
(1) 写出“酸溶”一步中,MgCO3和硫酸反应的离子方程式 。
(2) 滤渣2的主要成分有MnO2和_____________,写出生成MnO2的离子方程式____________________。
(3)“合成”时需通蒸汽至80 ℃,边加热边搅拌,温度控制在80 ℃的原因是________________________(只需写出相应的化学方程式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH3及其盐都是重要的化工原料。
(1)用NH4Cl和Ca(OH)2制备NH3,反应发生、气体收集和尾气处理装置依次为_____________。

(2)按下图装置进行NH3性质实验。
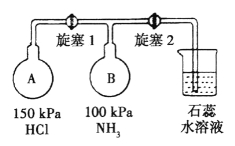
①先打开旋塞1,B瓶中的现象是_______________,原因是____________,稳定后,关闭旋塞1。
②再打开旋塞2,B瓶中的现象是_____________。
(3)设计实验,探究某一种因素对溶液中NH4Cl水解程度的影响。
限制试剂与仪器:固体NH4Cl、蒸馏水、100mL容量瓶、烧杯、胶头滴管、玻璃棒、药匙、天平、PH计、温度计、恒温水浴槽(可控制温度)
①实验目的:探究对溶液中NH4Cl水解程度的影响。
②设计实验方案,拟定实验表格,完整体现实验方案(列出能直接读取数据的相关物理量及需拟定的数据,数据用字母表示;表中V(溶液)表示所配制溶液的体积)。

③按实验序号I所拟数据进行实验,若读取的待测物理量的数值为Y,则NH4Cl水解反应得平衡转化率为______________ (只列出算式,忽略水自身电离的影响)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com