
| A. | 12.5% | B. | 25% | C. | 50% | D. | 75% |
分析 根据有机物燃烧的化学反应方程式,分析反应前后气体体积的变化,利用气体体积缩小了72mL及混合气体的体积来列等式计算出乙炔的体积,最后计算乙炔的体积分数.
解答 解:由乙烷、乙炔和丙烯燃烧的方程式可知,除去水蒸气,恢复到原来的温度和压强,
C2H6+$\frac{7}{2}$O2=2CO2+3H2O△V
1 $\frac{7}{2}$ 2 2.5
C2H2+$\frac{5}{2}$O2=2CO2+H2O?△V
1 $\frac{5}{2}$ 2 1.5
C3H6+$\frac{9}{2}$O2=3CO2+3H2O?△V
1 $\frac{9}{2}$ 3 2.5
则C2H6和C3H6反应后体积缩小的量是相同的,故可将两者看成是一种物质即可,
设C2H6和C3H6一共为xmL,C2H2为ymL,
则有$\left\{\begin{array}{l}{x+y=32}\\{2.5x+1.5y=72}\end{array}\right.$,解得y=8mL,
混合烃中乙炔的体积分数为$\frac{8}{32}×100%=25%$,
故选B.
点评 本题考查学生利用有机物燃烧的化学反应方程式进行体积分数的计算,侧重于学生的分析、计算能力的考查,明确气体体积缩小的量及将乙烷和丙烯看成一种物质是解答的关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 为除去FeCl2溶液中少量的FeCl3,可加入过量铁粉,再过滤 | |
| B. | 明矾中Al3+水解产生具有吸附性的胶体,明矾可用于自来水的净化 | |
| C. | 为除去CO2中少量的HCl,可使其通过饱和的Na2CO3溶液 | |
| D. | 为除去KCl溶液中少量的MgCl2,可加入适量KOH溶液,再过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 反应物 | 反应条件1 | 反应条件2 | |
| A | CH3CHICH3 | NaOH的水溶液,加热 | NaOH的乙醇溶液,加热 |
| B | 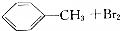 | 光照 | 铁粉 |
| C | 乙醇+氧 | 点燃 | Cu做催化剂,加热 |
| D | 乙烯 | 溴水 | 溴的四氯化碳溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Na+、SO42-、Cl2 | B. | Ca2+、Na+、Br-、CO32- | ||
| C. | Na+、Fe2+、Cl-、NO3- | D. | K+、Ag+、NH3•H2O、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 相同时间内CO2转化率 | T1 | T2 | T3 | T4 | T5 |
| 反应Ⅰ | 65% | 77% | 80% | 80% | 66.67% |
| 反应Ⅱ | 56% | 67% | 76% | 80% | 66.67% |
| 反应Ⅲ | 48% | 62% | 72% | 80% | 66.67% |
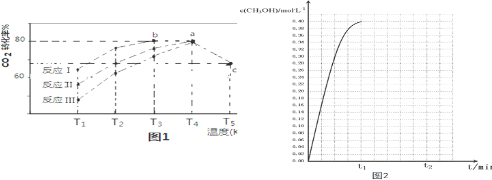
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 低温、高压、催化剂 | B. | 高温、高压 | ||
| C. | 尽可能的高温、高压 | D. | 适宜的温度、高压、催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
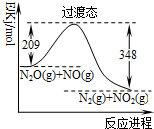
| A. | 使用催化剂可以降低过渡态的能量 | |
| B. | 反应物能量之和大于生成物能量之和 | |
| C. | N2O(g)+NO(g)→N2(g)+NO2(g)+139kJ | |
| D. | 反应物的键能总和大于生成物的键能总和 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com