
【题目】某有机物其结构如图所示,下列说法中正确的是()
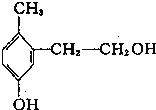
A.它是苯酚的同系物
B.1mol有机物能与2molNaOH反应
C.1mol该有机物能与金属钠反应产生![]()
D.1mol该有机物能与溴水反应消耗2mol![]() 发生取代反应
发生取代反应
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】己烷雌酚的一种合成路线如图:

下列说法不正确的是( )
A.化合物X难溶于水
B.在NaOH水溶液中加热,化合物X可发生取代反应
C.在一定条件,化合物Y可与CH3COOH发生缩聚反应
D.用FeCl3溶液可鉴别化合物X和Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】银白色固体A:①放在空气中可氧化生成白色固体B;②将A点燃,火焰呈黄色,生成淡黄色固体C;③A、B、C均可与无色液体D反应,生成碱性物质E,其中A跟D反应时还可以生成可燃性气体F,C跟D反应则生成另一种气体G;④F和G混合后遇火可剧烈反应而发生爆炸,并生成D。据此判断:
(1)A______,B______,C______,D________,E____,F_______,G_______。(填化学式)
(2)写出有关反应的化学方程式:
①___________________________________________。
②__________________________________________。
③__________________________________________。
④__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高氯酸盐(ClO4-)有高稳定性和强氧化性,常作为氧化剂用于工业生产。
(1)高氯酸盐中氯元素的化合价为________。
(2)下列叙述中可说明氯元素比硫元素非金属性强的是_________。
① HCl比H2S稳定
② HClO4的酸性比H2SO3的强
③ Cl2可与Na2S发生置换反应
(3)NH4ClO4是复合火箭推进剂的重要成分,实验室可通过反应NaClO4+NH4Cl![]() NH4ClO4+NaCl制取。相关物质的溶解度曲线如图:
NH4ClO4+NaCl制取。相关物质的溶解度曲线如图:
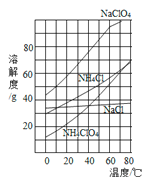
① 结合溶解度,分析该反应能够发生的原因________。
② 从反应后热的混合液中获得较多NH4ClO4晶体的实验操作依次为________、蒸发浓缩、冷却结晶、过滤、冰水洗涤。
(4)高氯酸盐是一种新型的无机污染物,ClO4-的主要危害是与碘离子竞争进入人体甲状腺,影响甲状腺的正常功能。利用电化学催化法,酸性环境中,可将ClO4-还原为Cl-,该电极反应式为________。
(5)已知,加热时Cu(ClO4)2的分解方式有以下两种:
2Cu(ClO4)2 ![]() 2CuO+7O2↑+2Cl2↑
2CuO+7O2↑+2Cl2↑
Cu(ClO4)2 ![]() CuCl2+4O2↑
CuCl2+4O2↑
取一定质量的Cu(ClO4)2·6H2O样品,加热至某温度使其完全分解,若测得V(O2)∶V(Cl2)=5∶1,则分解所得固体产物中CuO与CuCl2的物质的量之比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钢铁“发蓝”是指在钢铁的表面形成一层四氧化三铁的技术过程。其中第一步反应为:3Fe+ NaNO2+ 5 NaOH= 3Na2FeO2+ H2O+ NH3↑。关于该反应说法正确的是![]()
A.反应中N元素被氧化
B.NaFeO2既是氧化产物也是还原产物
C.整个反应过程中每有![]() 参加反应就转移
参加反应就转移![]() 电子
电子
D.氧化剂与还原剂的物质的量之比为3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家发现,食用虾类等水生甲壳类动物的同时服用维生素C容易中毒。这是因为对人体无害的![]() 价砷类化合物在维生素C的作用下,能够转化为有毒的
价砷类化合物在维生素C的作用下,能够转化为有毒的![]() 价的含砷化合物。通过以上信息填空:
价的含砷化合物。通过以上信息填空:
①维生素C具有______(填“氧化性”或“还原性”)。
②3mol +5价砷完全转化为![]() 价砷,共转移______个电子。
价砷,共转移______个电子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室以次氯酸盐和铁盐为原料制备少量K2FeO4的操作步骤如下:
Ⅰ.制备NaClO强碱性饱和溶液:
①将20 mL NaOH溶液加入仪器b中,冷水浴冷却,通入Cl2,搅拌,直至溶液变为黄绿色且有少量白色晶体析出为止(装置如下图所示)。

②将所得饱和NaClO倒入烧杯并置于冷水浴中,分几次加入20 g NaOH固体并不断搅拌,过滤,得NaClO强碱性饱和溶液。
(1)甲装置中a管的作用是_____________________________________________。
(2)写出甲装置中反应的化学方程式_____________________________________。
(3)石灰乳的作用是___________________________________________________。
(4)反应过程中用冷水浴冷却的原因是___________________________________。
Ⅱ.合成K2FeO4:
①称取5.05 g Fe(NO3)3·9H2O(相对分子质量为404)固体,在冷水浴中分批加入Ⅰ中所得滤液,并不断搅拌,反应1小时后溶液呈深紫红色(即Na2FeO4)。
②离心分离除去Na2FeO4水解得到的Fe(OH)3胶体,留上层清液(深紫红色)。
③向②的上层清液中缓慢加入KOH饱和溶液50.00mL,冰水浴保持5 min,过滤,得K2FeO4(相对分子质量为198)粗产品。
④将粗产品重结晶,并用异丙醇洗涤,低温烘干,得纯产品2.13 g。
(5)合成Na2FeO4的离子方程式为____________________________________。
(6)过程③加入饱和KOH溶液即可得到K2FeO4粗产品,原因是__________。
(7)用异丙醇洗涤的目的是__________________________________________。
(8)K2FeO4的产率为___________(保留至0.1%)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了确定某物质是否变质,所选试剂(括号内物质)达不到实验要求的是( )
A.K2SO3是否被氧化(BaCl2溶液)B.新制氯水已经完全变质(紫色石蕊试液)
C.KI是否被氧化(淀粉溶液)D.FeSO4是否被氧化(KSCN溶液)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com