
 2NH3(g)△H=-92kJ?mol-1;
2NH3(g)△H=-92kJ?mol-1;

 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:
| A、用氨水鉴别Al3+、Mg2+、Ag+ |
| B、向某溶液中加入2滴KSCN溶液,溶液不显红色.再向溶液中加入几滴新制的氯水,溶液变为血红色,该溶液中不一定含有Fe2+ |
| C、NaCl、FeCl2、FeCl3、MgCl2、AlCl3五种溶液,用烧碱溶液就可把它们鉴别开来 |
| D、要证明Fe3+溶液中含有Fe2+可以用NH4SCN溶液和氯水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只有AgBr沉淀生成 |
| B、AgCl和AgBr沉淀都有,但以AgCl沉淀为主 |
| C、AgCl和AgBr沉淀等量生成 |
| D、AgCl和AgBr沉淀都有,但以AgBr沉淀为主 |
查看答案和解析>>
科目:高中化学 来源: 题型:
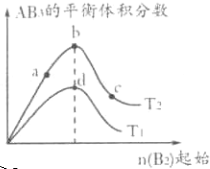
| A、若T2>T1,达到平衡时b、d点的反应速率为vd>vb |
| B、若T2>T1,则正反应一定是放热反应 |
| C、达到平衡时A2的转化率大小为b>a>c |
| D、在T2和n(A2)不变时达到平衡,AB3的物质的量大小为c>b>a |
查看答案和解析>>
科目:高中化学 来源: 题型:
 向盛有一定量浓度NaOH溶液的烧杯中通入一定量的CO2气体后得溶液M,向所得溶液M中逐滴加入稀盐酸至过量,并将溶液加热,产生气体与加入稀盐酸的物质的量的关系如图所示,则M中的主要溶质为( )
向盛有一定量浓度NaOH溶液的烧杯中通入一定量的CO2气体后得溶液M,向所得溶液M中逐滴加入稀盐酸至过量,并将溶液加热,产生气体与加入稀盐酸的物质的量的关系如图所示,则M中的主要溶质为( )| A、Na2CO3 |
| B、NaHCO3 |
| C、Na2CO3、NaOH |
| D、NaHCO3、NaOH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com