
【题目】下图虚线框中的装置可用来检验浓硫酸与木炭粉在加热条件下反应产生的所有气体产物,填写下列空白:
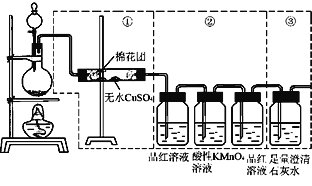
(1)浓硫酸与木炭粉在加热条件下的化学方程式为________________。
(2)如果装置中①、②、③三部分仪器的连接顺序改为②、①、③,则可以检验出的物质是________________;不能检出的物质是____________。
(3)如果将仪器的连接顺序变为①、③、②,则可以检出的物质是_____________;不能检出的物质是_____________。
【答案】C+ 2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O SO2、CO2 H2O H2O CO2、SO2
CO2↑+2SO2↑+2H2O SO2、CO2 H2O H2O CO2、SO2
【解析】
在加热条件下浓硫酸可将C氧化为CO2,浓硫酸被还原生成SO2,同时产生水,利用电子守恒、原子守恒书写方程式。要检验反应产生的物质,为防止用溶液检验时带出水,影响检验结果,要先通过无水硫酸铜检验水的存在,若固体由白色变为蓝色证明水的产生,由于二氧化硫、二氧化碳都能使澄清石灰水变浑浊,要先利用SO2的漂白性,用品红溶液检验SO2的存在,通过酸性KMnO4溶液除去SO2,再用品红溶液检验SO2已经除干净,最后用澄清石灰水检验CO2气体的存在,据此分析解答。
(1)浓硫酸具有强氧化性,在加热时能够将C氧化为CO2,浓硫酸本身被还原为SO2,同时产生水,根据电子守恒、原子守恒,可得相应的反应方程式为:C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O ;
CO2↑+2SO2↑+2H2O ;
(2)①中装有无水硫酸铜,无水硫酸铜遇水由白色变成蓝色的五水合硫酸铜,②中SO2能使品红溶液褪色,SO2也能使酸性高锰酸钾溶液褪色,③二氧化硫、二氧化碳都能使澄清石灰水变浑浊。如果装置中①、②、③三部分仪器的连接顺序改为②、①、③,通过②中品红溶液褪色,说明有SO2,通过酸性高锰酸钾溶液除去SO2,再通过品红溶液,品红不褪色,说明二氧化硫已经除尽,通过①中装有无水硫酸铜,无水硫酸铜遇水由白色变成蓝色的五水合硫酸铜,但不能说明是生成的水,可能是溶液中的水;通过③澄清石灰水,石灰水变浑浊,说明有二氧化碳生成,故可以检验出的物质是SO2和CO2;不能检验出的物质是H2O;
(3)如果将仪器的连接顺序变为①、③、②,通过①中装有无水硫酸铜,无水硫酸铜遇水由白色变成蓝色的五水合硫酸铜,能说明生成有水;通过③澄清石灰水,石灰水变浑浊,二氧化硫、二氧化碳都能使澄清石灰水变浑浊,因此不可以检出二氧化硫、二氧化碳的存在。


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案科目:高中化学 来源: 题型:
【题目】下列物质属于电解质且能导电的是( )
①氯化铜溶液 ②氯化铵固体 ③铜 ④石墨 ⑤熔融氢氧化钾 ⑥稀硫酸 ⑦酒精
A. ⑤B. ①②⑥C. ②⑤⑥⑦D. ①③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度和压强下,把装有NO和NO2的混合气体的试管倒立于水中,充分反应后,试管内气体的体积缩小为原气体体积的![]() ,则原混合气体中NO和NO2的体积比为( )
,则原混合气体中NO和NO2的体积比为( )
A. 3∶lB. 1∶3C. 2∶3D. 3∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取一定量的Fe、Cu的混合物粉末,平均分成A、B、C、D、E五等份,分别向每一份中加入一定量的稀硝酸,实验中收集到的NO气体(惟一还原产物)的体积及所得剩余物的质量记录如下(所有体积均在标准状况下测定):
实验序号 | A | B | C | D | E |
硝酸溶液体积 | 100ml | 200 mL | 300 mL | 400 mL | 500 mL |
剩余固体的质量 | 17.2 g | 8g | 0 g | 0 g | 0 g |
气体体积 | 2.24 L | 4.48 L | 6.72L | 7.84 L | 7.84 L |
(1)A组实验后17.2 g剩余固体为________,B组实验后8 g剩余固体为_______。(均填写化学式)
(2)实验中每次所取混合物中铁的物质的量为________mol。
(3)若C组金属恰好反应完,则反应后溶液中的金属阳离子为:_____________ ,物质的量之比是:________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可用如图装置制取、净化、收集气体的是
选项 | 气体 | ① | ② | ③ |
|
A | NH3 | 浓氨水 | 生石灰 | 浓硫酸 | |
B | SO2 | 浓硫酸 | Na2SO3 | 浓硫酸 | |
C | NO2 | 浓硝酸 | 铜屑 | H2O | |
D | Cl2 | 浓盐酸 | MnO2 | H2O |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯在饮用水处理中常用作杀菌剂,且HClO的杀菌能力比ClO-强。25℃时氯气-氯水体系中存在以下平衡关系:
Cl2(g)![]() Cl2(aq) K1=10-1.2
Cl2(aq) K1=10-1.2
Cl2(aq)+ H2O![]() HClO + H++Cl-K2=10-3.4
HClO + H++Cl-K2=10-3.4
HClO![]() H++ ClO-Ka=?
H++ ClO-Ka=?
其中Cl2(aq)、HClO和ClO-分别在三者中所占分数(α)随pH变化的关系如图所示。下列表述正确的是( )

A. Cl2(g)+ H2O![]() 2H++ ClO-+ Cl-K=10-10.9
2H++ ClO-+ Cl-K=10-10.9
B. 在氯处理水体系中,c(HClO) + c(ClO-) =c(H+)-c(OH-)
C. 用氯处理饮用水时,pH=7.5时杀菌效果比pH=6.5时好
D. 氯处理饮用水时,在夏季的杀菌效果比在冬季差
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.某同学帮助水质检测站配制480mL0.5mol·L-1NaOH溶液以备使用。
(1)其操作步骤如乙图所示,则甲图操作应在乙图中的______之间。
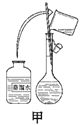
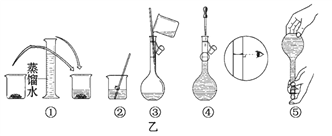
A.②与③ B.①与② C.③与④
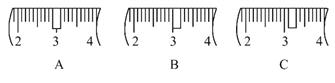
(2)该同学应称取NaOH固体________g,用质量为23.1 g的烧杯放在托盘天平上称取所需NaOH固体时,请在在下图中选出能正确表示游码位置的选项________(填字母)。
Ⅱ.现有下列A、B、C三种常用化学仪器,请回答下列有关问题:
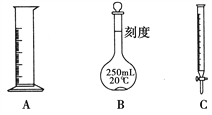
(1)三种化学仪器中标有“0”刻度的为________(填名称)。
(2)三种化学仪器在使用时首先需要检验是否漏液的为________(填字母代号)。
(3)用三种化学仪器中的一种对液体体积进行计量,正确的读数为n mL,仰视读数为x mL,俯视读数为y mL,若y>n>x,则所用量器是________(填名称)。
Ⅲ.化学课外活动小组设计了如下图所示的一套气体发生、收集和尾气吸收装置,以探究该装置的多功能性。
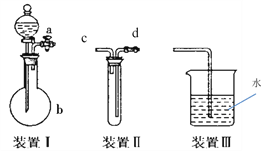
(1)实验前要检验装置Ⅰ的气密性,写出操作方法____________;
(2)利用装置Ⅱ可直接收集CO2,进气口为_____________。
(3)以上三个装置可组成实验室制取NH3,利用装置Ⅲ 吸收NH3时会发生倒吸,可向水中再加入一种液体可防止倒吸的发生,该液体为________(填化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com