
 SiF4(g)+ 2H2O(g) ΔH =" —148.9" kJ/mol
SiF4(g)+ 2H2O(g) ΔH =" —148.9" kJ/mol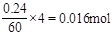 ,所以其反应速率是
,所以其反应速率是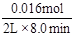 =0.001moL/(L·min)。
=0.001moL/(L·min)。

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:填空题
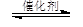 CH3CH2OH(g)+3H2O(g) 。
CH3CH2OH(g)+3H2O(g) 。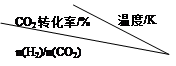 | 500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2.0 | 60 | 43 | 28 | 15 |
| 3.0 | 83 | 62 | 37 | 22 |
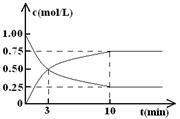
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
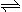 2NO2 (g) ΔH<0,
2NO2 (g) ΔH<0,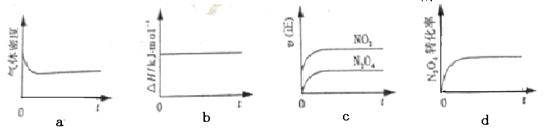
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
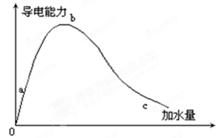
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:下列说法正确的是
PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:下列说法正确的是| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/ mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①③ | B.①④ | C.②③ | D.③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.生成1mol乙酸乙酯的同时,也生成1mol乙酸 |
| B.乙酸、乙醇、乙酸乙酯的浓度相同 |
| C.当乙酸断开1mol碳氧单键的同时,乙醇也断开了1mol氢氧键 |
| D.当乙酸断开1mol氢氧键的同时,乙醇也断开了1mol碳氧单键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2NO2 (g)在下列过程中发生的变化描述正确的是
2NO2 (g)在下列过程中发生的变化描述正确的是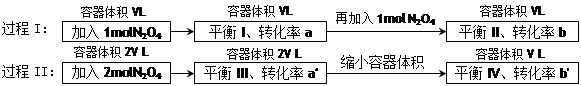
| A.a' < b'、a > b | B.在平衡I向平衡II过渡的过程中,v(逆) < v(正) |
| C.a' > a、b' < b | D.平衡II与平衡IV中N2O4的质量分数相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com