
【题目】已知苯甲酸的酸性比碳酸强,苯酚的酸性比碳酸弱。则可以将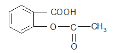 变为
变为![]() 的方法是
的方法是
①与足量的NaOH溶液共热,再通入CO2
②与稀硫酸共热后,加入足量的NaOH溶液
③与稀H2SO4共热后,加入足量的 NaHCO3
④与稀H2SO4共热后,加入足量的Na2CO3
A.①③B.①②C.①④D.②③
科目:高中化学 来源: 题型:
【题目】通过测定混合气中O2含量可计算已变质的Na2O2 (含Na2CO3) 纯度,实验装置如图(Q为弹性良好的气囊)。下列分析错误的是
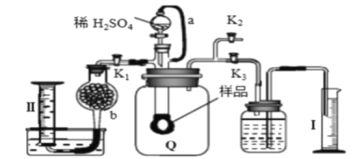
A. 干燥管b中装入碱石灰
B. Q气球中产生的气体主要成份O2、CO2
C. 测定气体总体积必须关闭K1、K2,打开K3
D. 读完气体总体积后,关闭K3,缓缓打开K1;可观察到Q气球慢慢缩小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国传统文化中包括许多科技知识。下列古语中不涉及化学变化的是( )
A.熬胆矾(CuSO4·5H2O)铁釜,久之亦化为铜B.千淘万漉虽辛苦,吹尽狂沙始到金
C.凡石灰(CaCO3)经火焚炼为用D.丹砂(HgS)烧之成水银,积变又成丹砂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室模拟合成氨和氨催化氧化的流程如下:
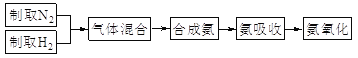
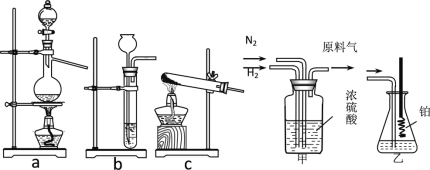
已知:实验室用饱和亚硝酸钠(NaNO2)溶液与饱和氯化铵溶液经加热后反应制取氮气。
(1)从图中选择制取气体的合适装置:氮气__、氢气___。
(2)氮气和氢气通过甲装置,甲装置的作用除了将气体混合外,还有__、_。
(3)用乙装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入乙装置的锥形瓶内,能使铂丝保持红热的原因是:_,锥形瓶中还可观察到的现象是:____。
(4)写出乙装置中氨氧化的化学方程式:_____。
(5)反应结束后锥形瓶内的溶液中含有H+、OH-、_、_离子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】蒽(![]() )与苯炔(
)与苯炔(![]() )反应生成化合物X(立体对称图形),如图所示:
)反应生成化合物X(立体对称图形),如图所示:

(1)蒽与X都属于___(填字母)。
a.饱和烃 b.不饱和烃
(2)苯炔的分子式为___,苯炔不具有的性质是___(填字母)。
a.能溶于水 b.能发生氧化反应 c.能发生加成反应 d.常温常压下为气体
(3)下列属于苯的同系物的是___(填字母,下同)。
A.![]() B.
B.![]()
C.![]() D.
D.![]()
(4)下列物质中,能发生加成反应,也能发生取代反应,同时能使溴水因加成反应而褪色,还能使酸性高锰酸钾溶液褪色的是___。
A.![]() B.C6H14 C.
B.C6H14 C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭系统中有反应C(s)+CO2(g)![]() 2CO(g),能使反应速率加快的措施是
2CO(g),能使反应速率加快的措施是
①通过减小容器体积增大压强 ②升高温度③将炭粉碎 ④通入CO2 ⑤增加炭的量 ⑥恒容条件下通入N2
A.①②③④B.①②④⑥C.①②③⑥D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高锰酸钾在化工医药、水处理等很多方面有重要应用,可以用电解法制备,装置如下。直流电源采用乙烷—空气的碱性燃料电池。下列说法不正确的是(已知电流效率η=![]() ×100%)
×100%)
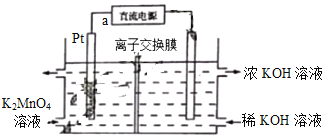
A. 电源负极的电极反应式为C2H6-14e-+18OH-=2CO32-+12H2O
B. 该离子交换膜为阴离子交换膜
C. a极为直流电源的正极
D. 若消耗0.02mo1![]() ,产生0.055mol
,产生0.055mol![]() ,则
,则![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知pC=-lgc(B),室温下,某二元酸(H2A)中部分微粒的pC值随溶液pH值变化关系如图所示。下列说法错误的是( )

A.曲线a表示的微粒是H+
B.溶液中水的电离程度:m>n
C.pH=8时,溶液中,c(HA-)>c(H2A)
D.pH=1与pH=3时,H2A的浓度几乎相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某课外小组设计的实验室制取乙酸乙酯的装置如下图所示。请回答:
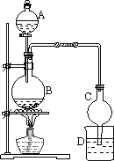
①若用 18O 标记乙醇中的氧原子,则 CH3CH218OH 与乙酸反应的化学方程式是_____________。
②球形干燥管C 的作用是______________。
③D 中选用饱和碳酸钠溶液的原因是_____________。
④反应结束后D 中的现象是_____________。
⑤下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有_____________(填序号)。
A.单位时间里,生成 1mol 乙酸乙酯,同时生成 1mol 水
B.单位时间里,消耗 1mol 乙醇,同时消耗 1mol 乙酸
C.正反应的速率与逆反应的速率相等
D.混合物中各物质的浓度不再变化
(2)N-苯基苯甲酰胺( 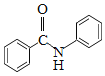 )广泛应用于药物,可由苯甲酸(
)广泛应用于药物,可由苯甲酸(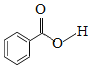 )与苯胺(
)与苯胺(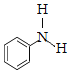 )反应制得,由于原料活性低,可采用硅胶催化、微波加热的方式,微波直接作用于分子,促进活性部位断裂,可降低反应温度。取得粗产品后经过洗涤—重结晶等,最终得到精制的成品。
)反应制得,由于原料活性低,可采用硅胶催化、微波加热的方式,微波直接作用于分子,促进活性部位断裂,可降低反应温度。取得粗产品后经过洗涤—重结晶等,最终得到精制的成品。
已知:
| 水 | 乙醇 | 乙醚 |
苯甲酸 | 微溶 | 易溶 | 易溶 |
苯胺 | 易溶 | 易溶 | 易溶 |
N-苯基苯甲酰胺 | 不溶 | 易溶于热乙醇,冷却后易 于结晶析出 | 微溶 |
下列说法不正确的是_____________(填字母编号)。
A.反应时断键位置为C—O 键和 N—H 键
B.洗涤粗产品用水比用乙醚效果更好
C.产物可选用乙醇作为溶剂进行重结晶提纯
D.硅胶吸水,能使反应进行更完全
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com