
胶体区别于其他分散系的本质特征是
A.胶体的分散质能通过滤纸孔隙,而浊液的分散质不能
B.胶体能产生丁达尔现象
C.胶体分散质粒子直径在1nm~100nm之间
D.胶体在一定条件下能稳定存在
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:
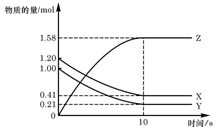
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如右图所示,下列描述正确的是 ( )
A.反应开始到10s,用Z表示的反应速率为0.158mol/(L·s)
B.反应开始到10s, X的物质的量浓度减少了0.79mol/L
C.反应开始时10s, Y的转化率为79.0%
D.反应的化学方程式为:X(g)+ Y(g) Z(g)
Z(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不能证明H2(g)+I2(g)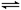 2HI(g)已达平衡状态的是
2HI(g)已达平衡状态的是
A.一个H—H 键断裂的同时有两个H—I键断裂
B.恒温恒容时,某一生成物浓度不再变化
C.恒温恒容时,混合气体颜色不再变化
D.恒温、压强一定,体积可变的容器,混合气体的密度不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
Q、R、X、Y、Z为周期表中原子序数依次递增的前四周期元素。
已知:①Q为元素周期表中原子半径最小的元素;②R的基态原子中电子占据三种能量不同的能级,且每种能级中的电子总数相同;③Y的基态原子的核外成对的电子数是未成对的电子数的3倍;④Z基态原子有六个未成对电子。用对应的元素符号或化学式回答下列问题:
(1)R、X、Y的第一电离能由大到小的顺序为 。
(2)Q元素在元素周期表中属于 区,与Y元素同族的第四周期元素的价电子排布式为 。
(3)RY2的电子式为 ,Z3+的原子结构示意图为____________。
(4)RQ2Y2的结构式为 ,m g该物质完全燃烧后通过足量Na2O2固体吸收,Na2O2固体增重的质量为 g。
(5)由Y、Z两种元素组成的Z2Y72-离子在酸性条件下可与乙醇反应,生成乙酸、Z3+等物质。该反应的离子方程式为__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海 水中提取的。某学校课外兴趣小组从海水晒盐后的盐卤(主要含Na+、Mg2+、Cl-、Br-等)中模拟工业生产来提取镁,主要过程如下:
水中提取的。某学校课外兴趣小组从海水晒盐后的盐卤(主要含Na+、Mg2+、Cl-、Br-等)中模拟工业生产来提取镁,主要过程如下:
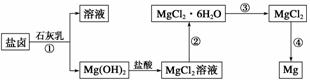
回答下列问题:
(1)工业上从盐卤中获取Mg(OH)2用石灰乳而不用NaOH溶液的原因是________________________________________________________________________。
(2)从过程①得到的Mg(OH)2沉淀中混有少量的Ca(OH)2,除去少量Ca(OH)2的方法是先将沉淀加入到盛有________溶液的烧杯中,充分搅拌后经________、______(填操作方法)可得纯净的Mg(OH)2。
(3)下图是该兴趣小组设计进行过程③的实验装置图:
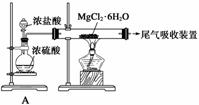
其中装置A的作用是____________________________________________________。
(4)写出过程④中发生反应的化学方程式___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列表格中各项都正确的一组是
| 类别 选项 | 碱 | 盐 | 电解质 | 非电解质 |
| A | 烧碱 | 小苏打 | BaSO4 | 干冰 |
| B | 纯碱 | CaCO3 | NH3·H20 | Fe |
| C | 明矾 | 食盐 | 石墨 | 醋酸 |
| D | KOH | CuSO4 | Na2SO4 | NaClO |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知A、B、C、D四种分子所含原子的数目依次为 1、3、6、6,且都含有18个电子,B、C是由两种元素的原子组成,且分子中两种原子的个数比均为1∶2。D是一种有毒的有机物。
(1)与组成A分子的原子的元素同族的上一周期的元素具有相同核外电子数的单核离子中,氧化性最强的 ,该离子与氢氧根离子结合生成的产物的电离方程式为 。
(2)从B分子的立体结构判断,该分子属于 分子(填“极性”或“非极性”)。B分子中心原子的最高价氧化物的浓溶液可以和B反应,写出该化学反应方程式并用单线桥标出电子转移的方向和数目 。
(3)C与另一种含有18个电子的4原子分子可以发生氧化还原反应,生成无污染的物质,该反应可以做为火箭发射原理,请写出该反应方程式 。
(4)D、氧气,氢氧化钠溶液和惰性电极可设计出一种燃料电池,则该燃料电池负极的电极反应式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com