
短周期主族元素X、Y、Z、W的原子序数依次增大。X原子的最外层电子数是其内层电子数的2倍,Y是地壳中含量最高的元素,Z2+与Y2-具有相同的电子层结构,W与Y同主族。下列说法正确的是( )
A.原子半径大小顺序:r(W)>r(Z)>r(Y)>r(X)
B.Y分别与Z、W形成的化合物中化学键类型相同
C.Y的气态简单氢化物的热稳定性比W的强
D.X的最高价氧化物对应水化物的酸性比W的强
科目:高中化学 来源: 题型:
可以验证硫元素的非金属性比氯元素弱的事实是 ( )
①H2S水溶液是弱酸,HCl水溶液是强酸 ②向氢硫酸溶液中滴入氯水有单质硫生成
③硫、氯气分别与铜和铁反应,其产物是FeS、Cu2S、FeCl3、CuCl2 ④高氯酸(HClO4)的酸性比硫酸强.
A.①②④ B.②④ C.②③④ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
世界环保联盟建议全面禁止使用氯气用于饮用水的消毒,而建议采用高效“绿色”消毒剂二氧化氯。二氧化氯是一种极易爆炸的强氧化性气体,易溶于水、不稳定、呈黄绿色,在生产和使用时必须尽量用稀有气体进行稀释,同时需要避免光照、震动或受热。实验室以电解法制备ClO2的流程如下:
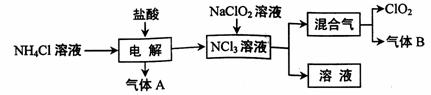
(1)ClO2中所有原子 (填“是”或“不是”)都满足8电子结构。上图所示方法制得的混合气中杂质气体B能使石蕊试液显蓝色,除去该杂质气体可选用 __;
A.饱和食盐水 B.碱石灰 C.浓硫酸 D.蒸馏水
(2)稳定性二氧化氯是为推广二氧化氯而开发的新型产品。下列说法正确的是 ;
A.二氧化氯可广泛用于工业和饮用水处理
B.应用在食品工业中能有效地延长食品贮藏期
C.稳定性二氧化氯的出现大大增加了二氧化氯的使用范围
D.在工作区和成品储藏室内,要有通风装置和监测及警报装置
(3)欧洲国家主要采用氯酸钠氧化浓盐酸制备,但该方法缺点是产率低、产品难以分离,还可能污染环境。写出该方法发生的化学方程式 ;
(4)我国广泛采用经干燥空气稀释的氯气与固体亚氯酸钠(NaClO2)反应制备,化学方程式是
,此法相比欧洲方法的优点是 。
(5)科学家又研究出了一种新的制备方法,利用硫酸酸化的草酸(H2C2O4)溶液还原氯酸钠,化学反应方程式为 ,此法提高了生产及储存、运输的安全性,原因是____ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各个曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。把与下面元素有关的性质相符的曲线标号填入相应的空格中:
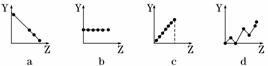
(1)ⅡA族元素的最外层电子数________;
(2)第3周期元素的最高化合价________;
(3)F-、Na+、Mg2+、Al3+的离子半径________。
查看答案和解析>>
科目:高中化学 来源: 题型:
0.2 mol有机物和0.4 mol O2在密闭容器中燃烧后的产物为CO2、CO和H2O(g)。产物经过浓硫酸后,浓硫酸的质量增加10.8 g;再通过灼热CuO充分反应后,固体质量减轻3.2 g;最后气体再通过碱石灰被完全吸收,碱石灰质量增加17.6 g。
(1)判断该有机物的化学式。
(2)若0.1 mol该有机物恰好与4.6 g金属钠完全反应,试确定该有机物的结构简式。(已知:一个碳上接两个羟基是不稳定的)
查看答案和解析>>
科目:高中化学 来源: 题型:
下面是四位同学在学习“化学反应的速率和化学平衡”一章后,联系工业生产实际所发表的观点,你认为不正确的是( )
A. 使用冰箱保存食物,是利用了化学反应速率理论
B. 化学平衡理论是研究怎样使用有限原料多出产品
C. 使用催化剂,可加快反应速率,目的是提高生产效率
D. 化学反应速率理论是研究怎样提高原料转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
锂离子电池已经成为应用最广泛的可充电电池。某种锂离子电池的结构示意图如图,其中两极区间的隔膜只允许Li+通过。电池充电时的总反应化学方程式为:LiCoO2 === Li1-xCoO2+xLi。关于该电池的推论错误的是( )
A.放电时,Li+主要从负极区通过隔膜移向正极区
B.放电时,负极反应xLi-xe-= xLi+
C.充电时,有电能转化为化学能
D.充电时,负极(C)上锂元素被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
2006年4月30日出现的亮菌甲素注射液引起多人中毒死亡的恶性事件。假药生产中原辅料中应有的“丙二醇”被换成廉价而有毒的化工原料“二甘醇”是致病人死亡的重要原因。二甘醇的结构简式是HO—CH2CH2—O—CH2CH2—OH。下列有关二甘醇的叙述正确的是 ( )
A.不能与金属钠发生反应 B.能发生取代反应
C.能溶于水,不溶于乙醇 D.符合通式Cn H2nO3
查看答案和解析>>
科目:高中化学 来源: 题型:
关于化学反应中的能量变化,下列说法中不正确的是( )
A.燃烧反应都是放热反应
B.对于可逆反应:aA(g)+bB(g)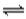 bC(g)+dD(g),如果正反应放热,逆反应一定吸热
bC(g)+dD(g),如果正反应放热,逆反应一定吸热
C.氢气燃烧生成水是一个放热的化学反应,说明1 mol H2的能量高于1 mol H2O的能量
D.只有放热的氧化还原反应才可以设计为原电池
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com