
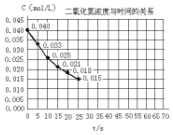
 二氧化氮在加热条件下能够分解成一氧化氮和氧气.该反应进行到45秒时,达到平衡(NO2浓度约为0.0125mol/L).图中的曲线表示二氧化氮分解反应在前25秒内的反应进程.
二氧化氮在加热条件下能够分解成一氧化氮和氧气.该反应进行到45秒时,达到平衡(NO2浓度约为0.0125mol/L).图中的曲线表示二氧化氮分解反应在前25秒内的反应进程.分析 (1)由图可知,20秒内NO2的浓度变化为0.04mol/L-0.018mol/L=0.022mol/L,根据v=$\frac{△c}{△t}$计算v(NO2),再利用速率之比等于化学计量数之比计算v(O2);
(2)化学平衡常数,是指在一定温度下,可逆反应达到平衡时各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,据此书写;
(3)二氧化氮在加热条件下能够分解成一氧化氮和氧气.该反应进行到45秒时,达到平衡(NO2浓度约为0.0125mol/L),图象分析可知,二氧化氮起始浓度0.04mol/L,结合三行计算列式得到,
2NO2?2NO+O2,
起始量(mol/L) 0.04 0 0
变化量(mol/L) 0.0275 0.0275 0.01375
平衡量(mol/L) 0.0125 0.0275 0.01375
在某温度下达到平衡后,不改变其它条件,向该容器中再加入少量的NO2,增大压强平衡正向进行,但加入量多于平衡移动减小的量,二氧化氮转化率减小,NO含量减小;
(4)若在反应开始时加入催化剂(其他条件都不变),反应速率加快,相同时间内NO2浓度变化量增大,到达平衡时间缩短,但不影响平衡移动,达到平衡是NO2浓度约为0.0125mol/L,据此用虚线画出加催化剂后的反应进程曲线.
解答 解:(1)由图可知,20秒内NO2的浓度变化为0.04mol/L-0.018mol/L=0.022mol/L,故v(NO2)$\frac{0.022mol/L}{20s}$=0.0011mol/(L•s),对于2NO2?2NO+O2,速率之比等于化学计量数之比,所以v(O2)=$\frac{1}{2}$v(NO2)=$\frac{1}{2}$×0.0011mol/(L•s)=5.5×10-4mol/(L•s),
故答案为:5.5×10-4;
(2)化学平衡常数,是指在一定温度下,可逆反应达到平衡时各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,对于可逆反应2NO2?2NO+O2的平衡常数k=$\frac{{c}^{2}(NO)c({O}_{2})}{{c}^{2}(N{O}_{2})}$,
故答案为:$\frac{{c}^{2}(NO)c({O}_{2})}{{c}^{2}(N{O}_{2})}$;
(3)二氧化氮在加热条件下能够分解成一氧化氮和氧气.该反应进行到45秒时,达到平衡(NO2浓度约为0.0125mol/L),图象分析可知,二氧化氮起始浓度0.04mol/L,结合三行计算列式得到,
2NO2?2NO+O2,
起始量(mol/L) 0.04 0 0
变化量(mol/L) 0.0275 0.0275 0.01375
平衡量(mol/L) 0.0125 0.0275 0.01375
在某温度下达到平衡后,不改变其它条件,向该容器中再加入少量的NO2,增大压强平衡正向进行,但加入量多于平衡移动减小的量,二氧化氮转化率减小,小于$\frac{0.0275mol/L}{0.04mol/L}$×100%=68.75%,NO含量减小;
故答案为:正反应方向,<,减小;
(4)若在反应开始时加入催化剂(其他条件都不变),反应速率加快,相同时间内NO2浓度变化量增大,到达平衡时间缩短,但不影响平衡移动,达到平衡是NO2浓度约为0.0125mol/L,据此用虚线画出加催化剂后的反应进程曲线为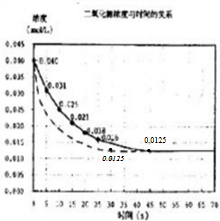 ,
,
故答案为: ;
;
点评 本题考查化学平衡速率的有关计算、平衡常数、影响反应速率与平衡移动的因素等,题目难度中等,注意基础知识的理解掌握.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 汽车制造商:车的外形变得美观,能够提高销量;易于加工,降低成本 | |
| B. | 车主:车的重量减轻,油耗降低;汽车价格便宜 | |
| C. | 意外被保险杠撞到的行人:具有缓冲作用,减轻伤害 | |
| D. | 旁观者:用塑料作保险杠不安全 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
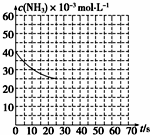 氨是最重要的化工产品之一.
氨是最重要的化工产品之一.| 弱电解质 | H2CO3 | NH3•H2O |
| 电离平衡常数 | Ka1=4.30×10-7 | 1.77×10-5 |
| Ka2=5.61×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\overline{v}$(O2)=0.3 mol•L-1•s-1 | B. | $\overline{v}$(NO)=0.24mol•L-1•s-1 | ||
| C. | $\overline{v}$(NH3)=0.12 mol•L-1•s-1 | D. | $\overline{v}$(H2O)=0.36mol•L-1•min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 其中氧化剂是MnO2,氧化产物是Cl2,氧化剂和还原剂物质的量之比是1:2.
其中氧化剂是MnO2,氧化产物是Cl2,氧化剂和还原剂物质的量之比是1:2.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 试剂 | 离子方程式 | |
| ①KCl (K2SO4) | ||
| ②Na2SO4 (MgSO4) | ||
| ③NaCl (Na2CO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用已知浓度的NaOH溶液测定未知浓度的醋酸溶液的浓度:H++OH-═H2O | |
| B. | 盛放NaOH溶液的试剂瓶不能用玻璃塞:SiO2+2Na++2OH-═Na2SiO3+H2O | |
| C. | 利用铝热反应焊接钢轨:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3 | |
| D. | 用氯水除去FeCl2溶液中的Fe2+:Cl2+Fe2+═2Cl-+Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
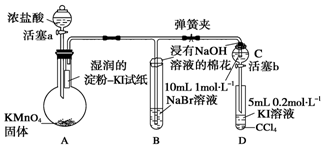
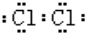 ;A中发生的反应的化学反应方程式为2KMnO4+16HCl═5Cl2↑+2MnCl2+2KCl+8H2O.
;A中发生的反应的化学反应方程式为2KMnO4+16HCl═5Cl2↑+2MnCl2+2KCl+8H2O.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com