
【题目】用酸性氢氧燃料电池电解粗盐水(含Na+、Cl-和少量Mg2+、Br-)的装置如图所示(a、b均为石墨电极),下列说法正确的是
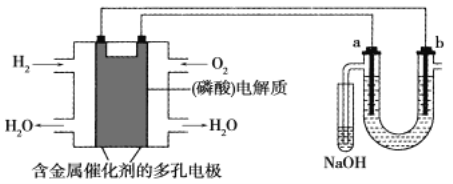
A.电池工作时,负极反应式为:H2-2e-+2OH-=2H2O
B.当电池中消耗2.24 L(标准状况下)H2时,b极周围会产生0.1 mol气体
C.电解过程中电子流动路径是:负极→外电路→阴极→溶液→阳极→正极
D.a极的电极反应式为:2H++2e-=H2↑
科目:高中化学 来源: 题型:
【题目】最近美国宇航局(NASA)马里诺娃博士找到了一种比二氧化碳有效104倍的“超级温室气体”全氟丙烷(C3F8),并提出用其“温室化火星”使其成为第二个地球的计划。有关全氟丙烷的说法正确的是( )
A.全氟丙烷(C3F8)分子中既有极性键又有非极性键
B.全氟丙烷(C3F8)的电子式为:
C.相同压强下,沸点:C3F8<C3H8
D.分子中三个碳原子可能处于同一直线上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相同温度下,下列有关反应速率的说法正确的是( )
A.![]() 的盐酸和
的盐酸和![]() 的硫酸分别与同体积
的硫酸分别与同体积![]() 的NaOH溶液反应的速率相同
的NaOH溶液反应的速率相同
B.等质量的大理石块和大理石粉分别与同体积![]() 盐酸反应的速率相同
盐酸反应的速率相同
C.等量的镁粉和铝粉分别与同体积![]() 的盐酸反应的速率相同
的盐酸反应的速率相同
D.![]() 的盐酸和
的盐酸和![]() 的硝酸与相同形状和大小的大理石反应的速相同
的硝酸与相同形状和大小的大理石反应的速相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 醋酸由于成本较低,在生产中被广泛应用。
(1)近年来化学家研究开发出用乙烯和乙酸为原料、杂多酸作催化剂合成乙酸乙酯的新工艺,不必生产乙醇或乙醛作中间体,使产品成本降低,具有明显经济优势。其合成的基本反应如下:CH2=CH2(g)+CH3COOH(l)![]() CH3COOC2H5(l)下列描述能说明恒温恒容条件下乙烯与乙酸合成乙酸乙酯的反应已达化学平衡的是________(填字母)。
CH3COOC2H5(l)下列描述能说明恒温恒容条件下乙烯与乙酸合成乙酸乙酯的反应已达化学平衡的是________(填字母)。
A.乙烯、乙酸、乙酸乙酯的浓度相同
B.酯化合成反应的速率与酯分解反应的速率相等
C.乙烯断开1mol碳碳双键的同时乙酸恰好消耗 1 mol
D.整个体系中乙烯的质量分数一定
E.气体的总压强不变
F.气体的摩尔质量不变
(2)在n(乙烯)与n(乙酸)物料比为1的条件下,某研究小组在不同压强下进行了在相同时间乙酸乙酯的产率随温度变化的测定实验,实验结果如图所示。回答下列问题:

①根据上图判断压强大到小的顺序是________,分析其原因_____。
②压强为p1、温度为60℃时,若乙酸的转化率为40%,则此时乙烯的转化率为____。
③在压强为p1、温度超过80℃时,分析乙酸乙酯产率下降的原因:_____
④根据测定实验结果分析,较适宜的生产条件是________(填出合适的压强和温度)。为提高乙酸乙酯的合成速率和产率,可以采取的措施有___________(任写出一条)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某试液中只可能含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 中的若干种离子,离子浓度均为
中的若干种离子,离子浓度均为![]() 某同学进行了如下实验:下列说法正确的是
某同学进行了如下实验:下列说法正确的是![]()

A.无法确定原试液中是否含有![]()
B.滤液X中大量存在的阳离子有![]() 、
、![]() 和
和![]()
C.沉淀C为Al![]()
D.原试液中一定不含有![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[Zn(CN)4]2-在水溶液中与HCHO发生如下反应:4HCHO+[Zn(CN)4]2+4H++4H2O= [Zn(H2O)4]2++4HOCH2CN,HOCH2CN的结构简式如下图所示,下列说法不正确的是

A. HOCH2CN分子中没有手性碳原子
B. 1mol HOCH2CN分子中含有σ键的物质的量为5mol
C. [Zn(CN)4]2-和[Zn(H2O)4]2+的中心原子配位数均为4
D. HOCH2CN分子中碳原子轨道的杂化类型分别是sp3和sp杂化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对某绿色溶液进行如下实验![]() 已知:
已知:![]() 微溶于水
微溶于水![]() :
:![]() 向溶液中滴加
向溶液中滴加![]() 溶液后,过滤,得到白色沉淀和绿色几乎不变的滤液:
溶液后,过滤,得到白色沉淀和绿色几乎不变的滤液:![]() 取滤液,再滴加
取滤液,再滴加![]() 溶液,有白色沉淀生成。下列说法正确的是
溶液,有白色沉淀生成。下列说法正确的是![]()
A.原溶液中一定存在![]() 、
、![]() 、
、![]() 中的一种或两种
中的一种或两种
B.原溶液中不能确定![]() 、
、![]() 、
、![]() 的存在
的存在
C.第![]() 步生成的白色沉淀是AgCl,没有
步生成的白色沉淀是AgCl,没有![]()
D.若原溶液中存在![]() 与
与![]() 中的一种或两种,可用NaOH溶液加以判断
中的一种或两种,可用NaOH溶液加以判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝及其化合物广泛应用于金属冶炼、有机合成等领域。
(1)铝热反应可以冶炼金属铬,Cr3+基态核外电子排布式为____________________。
(2)AlCl3可作反应的催化剂。

①1 mol对甲基苯乙酮分子中含有的σ键数目为__________。
②CH3COOH与H2O可以任意比例互溶,除因为它们都是极性分子外,还因为_______________。
(3)用价层电子对互斥理论解释SO![]() 的键角大于SO
的键角大于SO![]() 的原因是_______________。
的原因是_______________。
(4)某遮光剂的晶胞如图所示,由晶胞可知n=________。

(5)Na3[Co(NO2)6]常用作检验K+的试剂, 配位体![]() 的中心原子的杂化形式为______, 空间构型为_____。
的中心原子的杂化形式为______, 空间构型为_____。
大π键可用符号![]() 表示,其中m代表参与形成大π键的原子数,n为各原子的单电子数(形成σ键的电子除外)和得电子数的总和 (如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n为各原子的单电子数(形成σ键的电子除外)和得电子数的总和 (如苯分子中的大π键可表示为![]() ,则
,则![]() 中大π键应表示为__________。
中大π键应表示为__________。
(6)铁和氨气在640℃可发生置换反应,产物之一的晶胞结构如图所示,若该晶体的密度是ρg·cm-3,则两个最近的Fe原子间的距离为______cm。(阿伏加德罗常数用NA表示)

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在不同温度下,水溶液中![]() 与
与![]() 有如图所示关系。下列说法正确的是
有如图所示关系。下列说法正确的是![]()
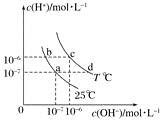
A.b点溶液中不可能存在![]()
B.b、c两点pH相同,但溶液的酸碱性不同
C.通过降温的方法,可使溶液的状态从d点变为a点
D.a点溶液中可能大量共存的离子:![]() 、
、![]() 、
、![]() 、
、![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com