
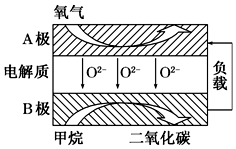
 �Լ���Ϊȼ�ϵ����͵�صõ��㷺���о�����ͼ��Ŀǰ�о��϶��һ�����������ȼ�ϵ�صĹ���ԭ��ʾ��ͼ������˵��������ǣ�������
�Լ���Ϊȼ�ϵ����͵�صõ��㷺���о�����ͼ��Ŀǰ�о��϶��һ�����������ȼ�ϵ�صĹ���ԭ��ʾ��ͼ������˵��������ǣ�������| A�� | �Լ���Ϊȼ�ϣ���ɱ�������������Ϊȼ�ϵĴ�ͳȼ�ϵ�� | |
| B�� | A�缫Ϊ���������������ԭ��Ӧ | |
| C�� | B�缫��ӦʽΪCH4+4O2--8e-�TCO2+2H2O | |
| D�� | ���ø�ȼ�ϵ������Դ����ʯī���缫���100 mL 1 mol•L-1������ͭ��Һ���������ռ���������������ʱ�����������ĵļ�������Ϊ22.4L����״���£� |
���� ���������ƶ������֪BΪ��������������������Ӧ�����鱻�������ɶ�����̼��ˮ���缫��ӦʽΪCH4+4O2--8e-�TCO2+2H2O��A�缫Ϊ���������������ԭ��Ӧ���缫��ӦʽΪO2+4e-�T2O2-���ݴ˷������
��� �⣺A����Ϊ����������õ����ɱ��ͣ������Լ���Ϊȼ�ϣ���ɱ�������������Ϊȼ�ϵĴ�ͳȼ�ϵ�أ���A��ȷ��
B��A�缫Ϊ���������������ԭ��Ӧ���缫��ӦʽΪO2+4e-�T2O2-����B��ȷ��
C��BΪ��������������������Ӧ���缫��ӦʽΪCH4+4O2--8e-�TCO2+2H2O����C��ȷ��
D������ͭ�����ʵ���=0.1L��1mol/L=0.1mol����ʼ�η�����Ӧ��2Cu2++2H2O$\frac{\underline{\;���\;}}{\;}$2Cu+O2��+4H+��ͭ������ȫ�ŵ������Ӧ2H2O$\frac{\underline{\;���\;}}{\;}$2H2��+O2�����������ռ���������������ʱ���������������������ȣ���������Ϊxmol�����ݵ���ת���غ㣬��0.1mol��2+2x=4x�����x=0.1��
���ݵ���ת���غ㣬��֪���ĵļ������ʵ���=$\frac{0.1mol��4}{8}$=0.05mol�������ļ�������=0.05mol��22.4L/mol=1.12L����D����
��ѡD��
���� �����ۺϿ���绯ѧ֪ʶ��Ϊ��Ƶ���㣬������ѧ���ķ��������������Ŀ��飬�����Ҫע�����ԭ��صĹ���ԭ�������յ缫����ʽ����д����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ʽΪC5H12���л��������֣����ǻ�Ϊͬϵ�� | |
| B�� | C4H8C12��9��ͬ���칹�壨�����������칹�� | |
| C�� | ʯ���͡������ķ���ϩ������ʹ��ˮ��ɫ | |
| D�� | �����ʵ����ļ�����������Ӧ��������ֲ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 100 mL 1 mol/L��FeCl3��Һ��ȫ����Fe��OH��3���壬�佺����ĿΪ0.1 NA | |
| B�� | 7.8 gNa2O2�к��е���������ĿΪ0.4 NA | |
| C�� | ��״���£�44.8 L HF����������Ϊ2 NA | |
| D�� | ��״���£�80 gSO3��������ԭ����Ϊ4 NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
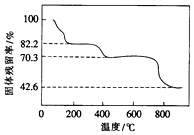 �������[Ce��SO4��2]��һ�ֳ��õ�ǿ��������
�������[Ce��SO4��2]��һ�ֳ��õ�ǿ��������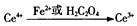
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ʵ�� | ���� | ���� | |
| A | �ô���ʯ�����ᷴӦ��ȡCO2���壬����ͨ��һ��Ũ�ȵ�Na2SiO3��Һ�� | ���ְ�ɫ���� | �ǽ����ԣ�Cl��C��S |
| B | ��ij��Һ�ȵμ������ữ���ٵμ�BaCl2��Һ | �а�ɫ�������� | ԭ��Һ�к���SO42-��SO32-��HSO32-�е�һ�ֻ��� |
| C | 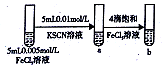 | �Թ�b���Թ�a����Һ�ĺ�ɫ�� | ����Ӧ��Ũ�ȣ�ƽ��������Ӧ�����ƶ� |
| D | 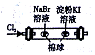 | ��������Ϊ��ɫ���ұ������Ϊ��ɫ | �����ԣ�Cl2��Br2��I2 |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| Ŀ�� | �Ŵ����� | ˵�� | |
| A | ʹ�� | ��������ú�����÷���ĵ�ÿǣ��ɻҡ���������ֽ�ôˡ��ҡ�����ˮŽ����Ƥ�ѽ��� | ���ҡ�����Ҫ�ɷ��������� |
| B | ���� | �����ޱ��ݡ�����ʯ��������ѩ������ǿ��֮���������𡱣�����������ʯ��KNO3����������Na2SO4�� | ������ɫ��Ӧ |
| C | ���� | �����������������һ�գ���ˮ�����գ���ȡ֭������֮���� | ��ȡ�������е���ά�� |
| D | ���� | �����ݸ�Ŀ����������ҩ����������KNO3������ǡ�ɼľ̿���ϣ���Ϊ���ݻ���ҩ�ߡ��� | ����KNO3�������� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ������ | B�� | Ԫ������ | C�� | ԭ�Ӱ뾶 | D�� | ���ϼ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ð�ˮ����Թܱڸ��ŵ����� | |
| B�� | ������������Һ��ϴմ��Ƥ���ϵı��� | |
| C�� | ��ʳ�����ůƿˮ������Ҫ�ɷ�̼��ƣ� | |
| D�� | ��̼������Һ���������Ʒ��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
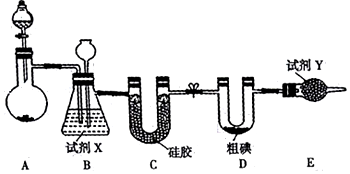
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com