
| A. | 水 | B. | 盐酸 | C. | 醋酸溶液 | D. | NaCl溶液 |
分析 溶液导电能力与离子浓度成正比,加入NaOH固体后溶液导电能力最小,说明该溶液中离子浓度最小,据此分析解答.
解答 解:A.水是弱电解质,溶液中离子浓度很小,NaOH是强电解质,在水溶液中完全电离,加入NaOH后,溶液中离子浓度增大较明显,所以导电能力变化较明显;
B.HCl是强电解质,在水溶液中完全电离,加入强电解质NaOH固体后,二者反应生成强电解质氯化钠,离子浓度几乎没有变化,导电能力变化不大;
C.醋酸是弱电解质,在水溶液中部分电离,加入强电解质NaOH固体后生成醋酸钠强电解质,溶液中离子浓度增大较明显,导电能力变化较明显;
D.NaCl是强电解质,在水溶液中完全电离,加入氢氧化钠固体后,二者不反应,溶液中离子浓度增大较明显,导电能力变化较明显;
通过以上分析知,溶液导电能力变化最小的是盐酸溶液,故选B.
点评 本题考查电解质溶液导电能力大小比较,明确电解质强弱及溶液导电能力影响因素是解本题关键,注意溶液导电能力与电解质强弱无关,与离子浓度、离子所带电荷有关,题目难度不大.


科目:高中化学 来源: 题型:填空题
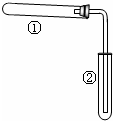 如图装置(夹持、加热装置已略)进行实验,有②中现象,不能证实①中反应发生的是( )
如图装置(夹持、加热装置已略)进行实验,有②中现象,不能证实①中反应发生的是( )| ①中实验 | ②中现象 |
| 铁粉与水蒸气加热 | 肥皂水冒泡 |
| 加热NH4Cl和Ca(OH)2混合物 | 酚酞溶液变红 |
| NaHCO3 | 澄清石灰水变浑浊 |
| 石蜡油在碎瓷片上受热分解 | Br2的CCl4溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 传统无机非金属材料是指:光导纤维、玻璃、水泥、陶瓷等硅酸盐材料 | |
| B. | 新型无机非金属材料虽然克服了传统无机非金属材料的缺点,但强度比较差 | |
| C. | 高温结构材料具有耐高温、耐酸碱腐蚀、硬度大、耐磨损、密度小等优点 | |
| D. | 传统无机非金属材料和新型无机非金属材料的主要成分都是硅酸盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 与
与 ⑥乙醇(CH3CH2OH)和甲醚(CH3OCH3);
⑥乙醇(CH3CH2OH)和甲醚(CH3OCH3); 和
和 ; ⑧
; ⑧ 和
和  .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
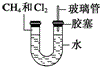 如图所示,U形管的左端被水和胶塞封闭有甲烷和氯气(体积比为1:4)的混合气体,假定氯气在水中的溶解度可以忽略.将封闭有甲烷和氯气的混合气体的装置放置在有光亮的地方,让混合气体缓慢地反应一段时间.
如图所示,U形管的左端被水和胶塞封闭有甲烷和氯气(体积比为1:4)的混合气体,假定氯气在水中的溶解度可以忽略.将封闭有甲烷和氯气的混合气体的装置放置在有光亮的地方,让混合气体缓慢地反应一段时间.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

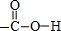
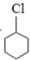 $\stackrel{②}{→}$
$\stackrel{②}{→}$ $\stackrel{③}{→}$Y$\stackrel{④}{→}$
$\stackrel{③}{→}$Y$\stackrel{④}{→}$
| 反应① | 反应② | 反应③ | |
| 试剂及条件 | |||
| 反应类型 |
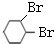 +2NaOH $→_{△}^{醇}$
+2NaOH $→_{△}^{醇}$ 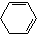 +2NaBr+2H2O
+2NaBr+2H2O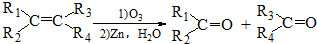 (R1、R2、R3、R4为烃基或H)
(R1、R2、R3、R4为烃基或H)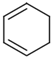 $→_{(2)Zn,H_{2}O}^{(1)O_{3}}$OHC-CH2CH2CHO+OHC-CHO,产物中含氧官能团的名称是醛基,
$→_{(2)Zn,H_{2}O}^{(1)O_{3}}$OHC-CH2CH2CHO+OHC-CHO,产物中含氧官能团的名称是醛基,查看答案和解析>>
科目:高中化学 来源: 题型:解答题
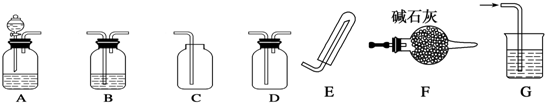
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+ HCO3- NO3- ClO- | B. | Na+ SO32- NH4+ Ba2+ | ||
| C. | Ba2+ S2- Cl- SO42- | D. | AlO2- CO32- Cl- Na+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com