
一般情况下,较强的氧化剂如:MnO2、KMnO4、KClO3、Ca(ClO)2等氧化浓盐酸时,有如下反应规律:氧化剂+浓盐酸→金属氯化物+水+氯气.实验室通常用该原理制取少量Cl2.现将214.5gCa(ClO)2放入500 mL 12.0 mol/L的浓盐酸中,生成的Cl2在标准状况下的体积为39.2 L.试计算:
(1)该反应消耗的氧化剂的质量是 g
(2)若反应前后溶液的体积保持不变,则反应后溶液中HCl的物质的量浓度为 .
考点: 化学方程式的有关计算.
分析: 由题可知,次氯酸钙与浓盐酸反应生成氯气(该反应属于归中反应),浓盐酸随着反应的进行会变成稀盐酸,即无法与次氯酸钙反应继续生成氯气了,只能生成次氯酸.通过题中给出的氯气的体积,可计算出消耗的HCl的物质的量,用反应前的浓盐酸中的HCl的物质的量减去前面消耗的HCl的物质的量,即可得出不再与次氯酸钙反应生成氯气时的剩余HCl的物质的量,由此分析解答.
解答: 解:(1)因为生成的Cl2在标准状况下的体积为39.2 L,n(Cl2)=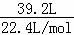 =1.75mol/L,依据化学方程式计算,
=1.75mol/L,依据化学方程式计算,
Ca(ClO)2+4HCl=CaCl2+2Cl2↑+2H2O
1 4 2
n(Ca(ClO)2) n1(HCl) 1.75mol
计算得到:n(Ca(ClO)2)=0.875mol;
n1(HCl)=3.5mol;所以氧化剂m(Ca(ClO)2)=0.875mol×143g/mol=125.1g,
答:该反应消耗的氧化剂的质量是125.1g;
(2)由(1)化学方程式计算只显酸性的氯化氢和次氯酸钙反应的氯化氢物质的量=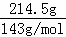 ﹣0.875 mol=0.625 mol
﹣0.875 mol=0.625 mol
Ca(ClO)2+2HCl=CaCl2+2HClO
1 2
0.625mol n2(HCl)
n2(HCl)=1.25 mol
反应后溶液中n(HCl)=0.5 L×12 mol/L﹣3.5 mol﹣1.25 mol=1.25 mol
c(HCl)= =2.5 mol/L;
=2.5 mol/L;
答:反应后溶液中HCl的物质的量浓度为2.5mol/L.
点评: 本题考查了氧化还原反应的规律分析判断,以及化学方程式计算,列关系式是解题关键,题目难度中等.


科目:高中化学 来源: 题型:
下列属于正确的水解离子方程式的是( )
|
| A. | NH4++H2O⇌NH3•H2O+H+ | B. | H2O+H2O⇌H3O++OH﹣ |
|
| C. | CO32﹣+2H2O⇌H2CO3+2OH﹣ | D. | Fe3++3H2O⇌Fe(OH)3↓+3H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知醋酸是日常生活中常见的弱酸。
(1)用pH试纸测定醋酸pH的操作是___________________________________
_______________________________________________________________________________________________________。
(2)常温下在pH=5的醋酸稀溶液中,醋酸电离出的c(H+)的精确值是________mol·L-1。
(3)用0.100 0 mol·L-1 NaOH溶液滴定20.00 mL某浓度的CH3COOH溶液,部分操作如下:
①取一支用蒸馏水洗净的碱式滴定管,加入标准氢氧化钠溶液,记录初始读数
②用酸式滴定管放出一定量待测液,置于用蒸馏水洗净的锥形瓶中,加入2滴甲基橙
③滴定时,边滴加边振荡,同时注视滴定管内液面的变化
请选出上述实验过程中的错误之处________(填序号)。上述实验与一定物质的量浓度溶
液配制实验中用到的相同仪器是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:还原性HSO3﹣>I﹣,氧化性IO3﹣>I2.在含0.3mol NaHSO3的溶液中逐滴加入KIO3溶液.加入KIO3和析出I2的物质的量的关系曲线如图所示.下列说法不正确的是()
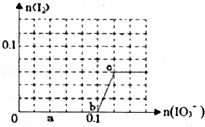
A. 0~b间的反应可用如下离子方程式表示:3HSO3﹣+IO3﹣═3SO42﹣+I﹣+3H+
B. a点时消耗NaHSO3的物质的量为0.12mol
C. 当溶液中I﹣与I2的物质的量之比为5:2时,加入的KIO3为0.18mol
D. b点时的还原产物可能是KI或NaI,b~c间的还原产物是I2
查看答案和解析>>
科目:高中化学 来源: 题型:
有以下几种物质①熔融氯化钠 ②浓硫酸 ③Cu ④蔗糖 ⑤CH3COOH ⑥NaHCO3 ⑦酒精 ⑧液溴,填空回答:(填序号)
(1)以上物质中属于强电解质的是 ; 属于非电解质的是 ;
(2)写出⑤⑥在水中的电离方程式:⑤ ;⑥ .
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,将气体X和气体Y各0. 16 mol充入2 L恒容密闭容器中,发生反应
X(g)+Y(g)=2Z(g) ,一段时间后达到平衡。反应过程中测定的数据如下表:
| t/min | 2 | 4 | 7 | 9 |
| n(X)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是( )
A、反应前2 min的平均速率ν(Z)=0.04mol/(L·min)
B.保持其他条件不变,若升高温度,平衡时c(X)= 0.06 mol·L-1,则该反应的H>0
C.相同温度下,起始时向容器中充入1mol X、0.2mol Y 和0.2mol Z,反应达到平衡前v(正)>v(逆)
D、其他条件不变,从反应体系中移走一部分 Z,正反应速率增大,逆反应速率减小,平衡正向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
某实验小组用下列装置进行乙醇催化氧化的实验。

图CB34
(1)实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学方程式:________________________________________________________________________;
在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明乙醇的氧化反应是________反应。
(2)甲和乙两个水浴作用不相同。甲的作用是________;乙的作用是________。
(3)反应进行一段时间后,试管a中能收集到不同的物质,它们是________________;集气瓶中收集到的气体的主要成分是________。
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有________。要除去该物质,可先在混合液中加入________(填写字母),然后再通过________(填实验操作名称)即可得到产物。
a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.四氯化碳
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com