
分析 由流程可知,Cr2O72-与亚铁离子发生氧化还原反应生成铁离子、铬离子,然后与石灰水反应转化为沉淀,从而达到废水处理的要求.
①结合电子、电荷守恒分析;
②结合c(Cr3+)及Ksp[Cr(OH)3]=c(Cr3+)c3(OH-)计算c3(OH-),再利用Ksp[Fe(OH)3]=c(Fe3+)c3(OH-)计算的c(Fe3+).
解答 解:由流程可知,Cr2O72-与亚铁离子发生氧化还原反应生成铁离子、铬离子,然后与石灰水反应转化为沉淀,从而达到废水处理的要求.
①绿矾化学式为FeSO4•7H2O,反应(I)发生氧化还原反应,由电子和电荷守恒可知离子方程式为Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O,
故答案为:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O;
②若处理后的废水中c(Cr3+)=3.0×10-6 mol•L-1,Ksp[Cr(OH)3]=6.0×10-31,
则c3(OH-)=$\frac{6.0×1{0}^{-31}}{3.0×1{0}^{-6}}$=2.0×10-25,
由Ksp[Fe(OH)3]=4.0×10-38可知,c(Fe3+)=$\frac{4.0×1{0}^{-38}}{2.0×1{0}^{-25}}$=2.0×10-13mol/L,
故答案为:2.0×10-13.
点评 本题考查混合物分离提纯及溶度积计算,为高频考点,把握流程中的反应及Ksp的计算为解答的关键,侧重分析与计算、实验能力的考查,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 2mL 0.1mol/L的NaOH溶液中滴加2滴0.1mol/L的MgCl2溶液,再滴加2滴0.1mol/L的FeCl3溶液 | 白色沉淀变为红褐色 | Ksp[Mg(OH)2]>Ksp[Fe(OH)3] |
| B | 常温下,质量与表面积均相同的铝片分别投入足量的稀、浓硫酸中 | 浓硫酸中铝片先溶解完 | 反应物浓度越大,反应速率越快 |
| C | 将KI和FeCl3溶液在试管中混合后,加入CCl4,振荡、静置 | 下层溶液显紫红色 | 氧化性:Fe3+>I2 |
| D | 向Na2SO3溶液加入稀盐酸酸化的Ba(NO3)2溶液 | 产生白色沉淀 | Na2SO3溶液已变质 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
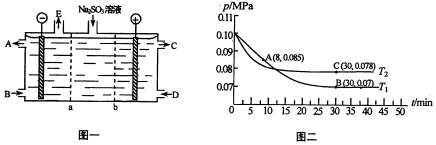
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
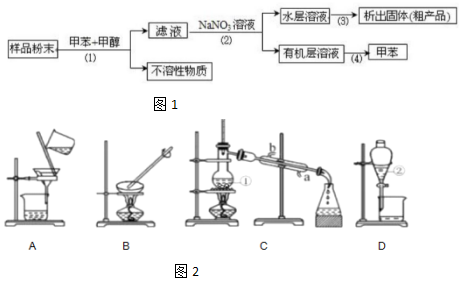
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
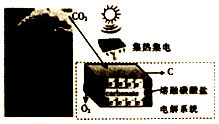 最近美国科学家实施了一项“天空绿色计划”,通过电解二氧化碳得到碳材料(部分原理如图所示),并利用得到的碳材料生产锂离子电池.下列说法正确的是( )
最近美国科学家实施了一项“天空绿色计划”,通过电解二氧化碳得到碳材料(部分原理如图所示),并利用得到的碳材料生产锂离子电池.下列说法正确的是( )| A. | 图中能量化方式只有一种 | |
| B. | 阳极的电极反应式为2CO32--4e-=2CO2↑+O2↑ | |
| C. | 若反应中转移1mole-,则理论上消耗CO32-0.5mol | |
| D. | 当生成12g碳材料时,可收集到22.4L O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
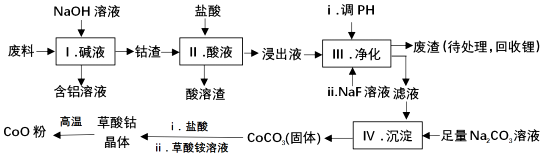
| Fe3+ | Co2+ | Co3+ | Al3+ | |
| pH(开始沉淀) | 1.9 | 7.15 | -0.23 | 3.4 |
| pH(完全沉淀) | 3.2 | 9.15 | 1.09 | 4.7 |
| 温度范围/℃ | 固体质量/g |
| 150~210 | 4.41 |
| 290~320 | 2.41 |
| 890~920 | 2.25 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com