
����Ŀ����A��B��C��D��E��F���ֶ�����Ԫ�أ���Ԫ��������Ϣ���£�A�ĵ������ܶ���С�����ʣ�B�ĵ���������ˮ���ҷ�Ӧ������ǿ������Һ�к������ֵ�������ͬ�����������ӣ�C��ԭ�����������������ڲ��������������D��Bͬ���ڣ���������D�ļ����Ӱ뾶��С��B��C��E��ɵ�36���ӵĻ�����Y�Ǽ�������������Ҫ�ɷ֣�FԪ���������������۵Ĵ�����Ϊ4��
��1��д�����־���A��B��C��F����Ԫ�صĻ���������Һ�����Ӧ�����ӷ���ʽ ��
��2��D��E��F�ļ����Ӱ뾶�ɴ�С��˳���ǣ�ֱ���û�ѧʽ��ʾ�� ��
��3����Fe��D������ɵĻ�����У���������F������������Ӧˮ�����ϡ��Һ������ȫ���ܽ⣮�����õ���Һ�м������������������Һ���������ij������˳�������ϴ�ӡ�������պ�õ�һ�ֹ��壬���������ָù����������ԭ����������ǡ����ȣ���ԭ�������D���ʵ���������Ϊ ��
��4��һ������ʯ������ͨ��һ������E���ʣ�����ǡ����ȫ��Ӧ���������������ֺ�EԪ�ص����ӣ������������ӵ����ʵ�����n���뷴Ӧʱ�䣨t����������ͼ��ʾ��t2ʱ��Ӧ�Ļ�ѧ����ʽΪ �� 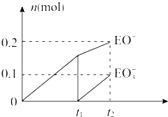
��5��A��B�γɵĻ�����BA���л��ϳ�����;�ܹ㷺�������Զ�ȡ�ܶ�����е����Ӷ�������Ӧ���ƵĻ����д�������Ҵ���Ӧ�Ļ�ѧ����ʽ ��
���𰸡�
��1��H++HSO3��=SO2��+H2O
��2��S2����Cl����Al3+
��3��30%
��4��10Cl2+10Ca��OH��2=7CaCl2+2Ca��ClO��2+Ca��ClO3��2+10H2O
��5��NaH+CH3CH2OH��CH3CH2ONa+H2��
���������⣺������Ԫ���У�A�ĵ������ܶ���С�����ʣ���AΪHԪ�أ�B�ĵ���������ˮ���ҷ�Ӧ������ǿ������Һ�к������ֵ�������ͬ�����������ӣ���BΪNa��C��ԭ�����������������ڲ��������������ԭ��ֻ����2�����Ӳ㣬����������Ϊ6����CΪOԪ�أ�D��B��Na��ͬ���ڣ���������D�ļ����Ӱ뾶��С����DΪAl��B��C��E��ɵ�36���ӵĻ�����Y�Ǽ�������������Ҫ�ɷ֣���EΪCl��YΪNaClO��FԪ���������������۵Ĵ�����Ϊ4����FΪSԪ�أ���1�����־���H��Na��O��S����Ԫ�صĻ�����ΪNaHSO4��NaHSO3 �� ����Һ�����Ӧ�����ӷ���ʽΪ��H++HSO3��=SO2��+H2O�����Դ��ǣ�H++HSO3��=SO2��+H2O����2�����Ӳ�ṹ��ͬ�����ӣ��˵����Խ�����Ӱ뾶ԽС�����ӵ��Ӳ�Խ�࣬���Ӱ뾶Խ�����Ӱ뾶��S2����Cl����Al3+ �� ���Դ��ǣ�S2����Cl����Al3+����3����Fe��Al������ɵĻ�����У���������ϡ���ᣬ����ȫ���ܽ⣮�����õ���Һ�м������������������Һ���������ij������˳�������ϴ�ӡ�������պ�õ�һ�ֹ���Ϊ��������������������������������ԭ����������ǡ����ȣ��������������൱����Ԫ�ص���������ԭ�������Al���ʵ���������������������OԪ�ص���������= ![]() ��100%=30%�����Դ��ǣ�30%����4������ͼ��֪������������ӵ����ʵ���Ϊ0.2mol����������ӵ����ʵ���Ϊ0.1mol�����Դ���������ӵ����ʵ�������������ӵ����ʵ���֮��Ϊ2��1�����ݵ�ʧ�����غ�֪���������������Ƶķ�Ӧ����ʽΪ��10Cl2+10Ca��OH��2=7CaCl2+2Ca��ClO��2+Ca��ClO3��2+10H2O�����Դ��ǣ�10Cl2+10Ca��OH��2=7CaCl2+2Ca��ClO��2+Ca��ClO3��2+10H2O����5��H��Na�γɵĻ�����NaHBA���л��ϳ�����;�ܹ㷺�������Զ�ȡ�ܶ�����е����Ӷ�������Ӧ���ƵĻ���������Ҵ���Ӧ�Ļ�ѧ����ʽΪ��NaH+CH3CH2OH��CH3CH2ONa+H2�������Դ��ǣ�NaH+CH3CH2OH��CH3CH2ONa+H2����
��100%=30%�����Դ��ǣ�30%����4������ͼ��֪������������ӵ����ʵ���Ϊ0.2mol����������ӵ����ʵ���Ϊ0.1mol�����Դ���������ӵ����ʵ�������������ӵ����ʵ���֮��Ϊ2��1�����ݵ�ʧ�����غ�֪���������������Ƶķ�Ӧ����ʽΪ��10Cl2+10Ca��OH��2=7CaCl2+2Ca��ClO��2+Ca��ClO3��2+10H2O�����Դ��ǣ�10Cl2+10Ca��OH��2=7CaCl2+2Ca��ClO��2+Ca��ClO3��2+10H2O����5��H��Na�γɵĻ�����NaHBA���л��ϳ�����;�ܹ㷺�������Զ�ȡ�ܶ�����е����Ӷ�������Ӧ���ƵĻ���������Ҵ���Ӧ�Ļ�ѧ����ʽΪ��NaH+CH3CH2OH��CH3CH2ONa+H2�������Դ��ǣ�NaH+CH3CH2OH��CH3CH2ONa+H2����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����״��������4.48L CH4����6.02��1023��HCl����13.6g H2S����0.3molNH3�����ж���������Ĺ�ϵ��С�����ʾ����ȷ����
A. ��� �٣��ܣ��ۣ��� B. �ܶ� �٣��ܣ��ۣ���
C. ���� �٣��ܣ��ۣ��� D. ��ԭ�����٣��ܣ��ۣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��ӦN2+3H2�T2NH3�������仯��ͼ��ʾ���÷�Ӧ���Ȼ�ѧ����ʽ�ǣ� �� 
A.N2��g��+3H2��g���T2NH3��l������H=2��a��b��c�� kJ/mol
B.N2��g��+3H2��g���T2NH3��g������H=2��b��a�� kJ/mol
C.![]() N2��g��+
N2��g��+ ![]() H2��g���TNH3��l������H=��b+c��a�� kJ/mol
H2��g���TNH3��l������H=��b+c��a�� kJ/mol
D.![]() N2��g��+
N2��g��+ ![]() H2��g���TNH3��g������H=��a+b�� kJ/mol
H2��g���TNH3��g������H=��a+b�� kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����10 mLŨ�Ⱦ�Ϊ3 mol��L��1��HNO3��H2SO4�Ļ����Һ�м���1.92 gͭ����ַ�Ӧ������Һ�����Ϊ10 mL����
��1�������������ڱ�״���µ�����Ƕ�������__________
��2����Ӧ����Һ�и����ʵ�����Ũ���Ƕ��٣�_____________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2L�ܱ�������ͨ��a mol����A��b mol����B����һ�������·�����Ӧ��mA��g��+nB��g��pC��g��+qD��g��
��֪��AΪ��ɫ���壻ƽ����Ӧ����vC= ![]() vA����Ӧ2minʱ��A��Ũ�ȼ�����ԭ����
vA����Ӧ2minʱ��A��Ũ�ȼ�����ԭ���� ![]() ��B�����ʵ���������
��B�����ʵ��������� ![]() mol����a mol D���ɣ�
mol����a mol D���ɣ�
�ش��������⣺
��1����Ӧ2min�ڣ�vA= �� vB= ��
��2����ѧ����ʽ�У�m= �� n= �� p= �� q= ��
��3����Ӧƽ��ʱ��DΪ2a mol����B��ƽ��ת����Ϊ ��
��4������ѡ����˵���÷�Ӧ�Ѿ��ﵽƽ��״̬����
A.�����ڵ�ѹǿ���ٱ仯
B.��ϵ���ܶȲ���
C.�������������������
D.A��B��C��D�����ʱ�ǡ��Ϊ�仯ѧ������֮��
E.����������ɫ���ٸı�
F.��������ƽ����Է����������ٸı�
G.vB������=vC���棩 ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������0.5mol/L��NaOH��Һ240ml������ʱӦѡ������ƿ�Ĺ��ͳ�ȡNaOH�������ֱ��ǣ� ��
A. 240ml��4.8gB. 250ml��5.0g
C. 250ml��4.8gD. ������4.8g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ҫ��ͭƬ�϶���ʱ�����������д�����ǣ� ��
�ٽ�ͭƬ���ڵ�Դ������ �ڽ���Ƭ���ڵ�Դ������ ����ͭƬ�Ϸ����ķ�Ӧ�ǣ�Ag++e���TAg ������Ƭ�Ϸ����ķ�Ӧ�ǣ�4OH����4e���TO2+2H2O �ݿ���CuSO4��Һ���������Һ ����AgNO3��Һ���������Һ��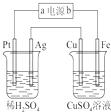
A.�٢ۢ�
B.�ڢۢ�
C.�٢ܢ�
D.�ڢۢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���E��C6H8O4���㷺Ӧ����Ϳ����ҵ�У�ijͬѧ�������·�ߺϳ�E������A����Է���������56��B����Է���������A��69����![]()
��1����A�ķ���ʽ�� ��
��2���۵ķ�Ӧ��������Ӧ��
��3����֪EΪ˳ʽ�ṹ�����ýṹ��ʽ��ʾ��ṹ�� ��
��4������˵����ȷ����������ţ���a����Ӧ������ȡ����Ӧ b��B����ȼ��黥Ϊͬϵ��
c��C������������ͬ���칹�� d��D�ܷ������۷�Ӧ
��5����Cת��ΪD��������4����Ӧ��ɣ�C ![]()
![]()
![]()
![]() D�������������Լ�����Ӧ���������ܵĻ�ѧ����ʽ�� ��
D�������������Լ�����Ӧ���������ܵĻ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪Ba��AlO2��2������ˮ����ͼ��ʾ������Al2��SO4��3��Һ����μ���Ba��OH��2��Һʱ�����ɳ��������ʵ���y�����Ba��OH��2�����ʵ���x�Ĺ�ϵ�������й�����������ǣ� �� 
A.a��bʱ���������ʵ�����Al��OH��3��BaSO4��
B.b��cʱ��Һ�����ӵ����ʵ�����AlO2����Ba2+��
C.a��dʱ���������ʵ�����Al��OH��3һ��С��BaSO4
D.d��eʱ��Һ�����ӵ����ʵ�����Ba2+���ܵ���AlO2��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com