
| ||
| A、S是氧化剂,KOH是还原剂 |
| B、若3mol硫完全反应,则反应中共转移了4mol电子 |
| C、还原剂与氧化剂的质量比是1:2 |
| D、氧化产物和还原产物的物质的量之比为3:2 |
| ||


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、入住前房间内保持一定温度并通风 |
| B、装修尽可能选择温度较高的季节 |
| C、请环境监测部门监测室内甲醛含量低于国家标准后入住 |
| D、紧闭门窗一段时间后入住 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、过氧化钠加入盐酸:2O22-+4H+=2H2O+O2↑ |
| B、金属铝溶于氢氧化钠溶液:Al+2OH-=AlO2-+H2↑ |
| C、AlCl3溶液中滴入氨水:Al3++3OH-=Al(OH)3↓ |
| D、Al(OH)3中滴加盐酸:Al(OH)3+3H+=Al3++3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,2.7g铝与足量的浓硫酸反应,失去的电子数为0.3NA |
| B、0.1mol/L的氢氧化钠溶液中含钠离子数为0.1NA个 |
| C、标准状况下,0.3 mol 双氧水中含有电子数为5.4NA |
| D、1molCH4与1mol NH4+所含质子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH3COOH分子不可能存在于pH>7的碱性溶液中 |
| B、等浓度的 (NH4)2CO3、(NH4)2SO4、(NH4)2Fe(SO4)2溶液中,c(NH4+)浓度依次增大 |
| C、将pH=2的盐酸和pH=4的盐酸等体积混合后,溶液的pH为3 |
| D、pH=5的盐酸溶液稀释1000倍,溶液的pH等于8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
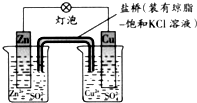
| A、负极反应为:Zn-2e-=Zn2+ |
| B、电池反应为:Zn+Cu2+=Zn2++Cu |
| C、在外电路中,电流从负极流向正极 |
| D、盐桥中的K+移向CuSO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
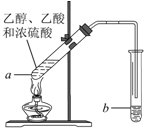 红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了有香味的酯.在实验室也可以用如图所示的装置制取乙酸乙酯,请回答下列问题.
红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了有香味的酯.在实验室也可以用如图所示的装置制取乙酸乙酯,请回答下列问题.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com