
·ÖĪö 25”ꏱ£¬c£ØOH-£©=c£ØH+£©=10-7mol/L£¬½įŗĻN=nNA”¢V=$\frac{m}{¦Ń}$¼ĘĖć£®
½ā“š ½ā£ŗ25”ꏱ£¬c£ØOH-£©=c£ØH+£©=10-7mol/L£¬10LĖ®ÖŠŗ¬ÓŠOH-µÄĪļÖŹµÄĮæĪŖ10L”Į10-7mol/L=10-6mol£¬ŗ¬H+µÄøöŹżĪŖ10-6mol”ĮNA=10-6NAøö£¬1gĖ®µÄĢå»żĪŖ1mL£¬Ōņ1gĖ®ÖŠŗ¬H+µÄøöŹżĪŖ1mL”Į10-3L”Į10-7mol/L”ĮNA=10-10NA£¬
¹Ź“š°øĪŖ£ŗ10-6£»10-6NA£»10-10NA£®
µćĘĄ ±¾Ģāæ¼²éĪļÖŹµÄĮæµÄ¼ĘĖć£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕ³£ĪĀĻĀc£ØOH-£©=c£ØH+£©=10-7mol/LĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓė¼ĘĖćÄÜĮ¦µÄ漲飬עŅā»ł±¾¼ĘĖć¹«Ź½µÄÓ¦ÓĆ£¬ĢāÄæÄŃ¶Č²»“ó£®


 A¼Ó½šĢā ĻµĮŠ“š°ø
A¼Ó½šĢā ĻµĮŠ“š°ø Č«ÓŲāŹŌ¾ķĻµĮŠ“š°ø
Č«ÓŲāŹŌ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CN-æÉŅŌŗĶĻ”ĮņĖį·“Ӧɜ³ÉHCN | B£® | CN-æɱ»Cl2Ńõ»Æ³É£ØCN£©2 | ||
| C£® | ŌŚĖ®ČÜŅŗÖŠ£ØCN£©2²»Äܽ«F-Ńõ»Æ | D£® | HCNµÄµē×ÓŹ½ĪŖ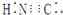 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ōµē³ŲŹĒ½«»ÆѧÄÜ×Ŗ»ÆĪŖµēÄܵÄ×°ÖĆ£¬¶ųµē½ā³ŲŹĒ½«µēÄÜ×Ŗ»ÆĪŖ»ÆѧÄܵÄ×°ÖĆ | |
| B£® | µē½ā³ŲµÄŠĪ³ÉĢõ¼žÖŠŅŖĒó±ŲŠėÓŠµēŌ“£¬Ōµē³ŲµÄŠĪ³ÉĢõ¼žÖŠ²»ŅŖĒóÓŠµēŌ“ | |
| C£® | Ōµē³ŲµÄøŗ¼«ŗĶµē½ā³ŲµÄŅõ¼«·¢ÉśµÄ·“Ó¦ĄąŠĶŅ»Ńł£¬¶¼ŹĒŃõ»Æ·“Ó¦ | |
| D£® | Ōµē³ŲµÄÕż¼«ŗĶµē½ā³ŲµÄŅõ¼«¶¼ŹĒµē×ÓĮ÷ČėµÄŅ»¼« |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ČĖĢåŗō³öµÄĘųĢåÖŠŗ¬ÓŠCO2£¬ĀĢÉ«Ö²ĪļµÄ¹āŗĻ×÷ÓĆĪüŹÕCO2£¬CO2ŹĒŅ»ÖÖÓŠ»ś»ÆŗĻĪļ | |
| B£® | Ė®ŹĒÉśĆüÖ®Ō“£¬H2OŹĒŅ»ÖÖÓŠ»ś»ÆŗĻĪļ | |
| C£® | ¾ų“󶹏żµÄŗ¬Ģ¼ĪļÖŹŹĒÓŠ»ś»ÆŗĻĪļ | |
| D£® | ÓŠ»ś»ÆŗĻĪļæÉŅŌ×Ŗ»ÆĪŖĪŽ»ś»ÆŗĻĪļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 6 | B£® | 12 | C£® | 18 | D£® | 24 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
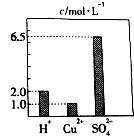 ŌŚ0.2LÓÉH2SO4”¢CuSO4ŗĶAl2£ØSO4£©3×é³ÉµÄ»ģŗĻČÜŅŗÖŠ£¬²æ·ÖĄė×ÓÅØ¶Č“óŠ”ČēĶ¼ĖłŹ¾£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
ŌŚ0.2LÓÉH2SO4”¢CuSO4ŗĶAl2£ØSO4£©3×é³ÉµÄ»ģŗĻČÜŅŗÖŠ£¬²æ·ÖĄė×ÓÅØ¶Č“óŠ”ČēĶ¼ĖłŹ¾£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ļ”ĻõĖįŗĶ¹żĮæĢśŠ¼·“Ó¦£ŗ3Fe+8H++2NO3-ØT3Fe2++2NO”ü+4H2O | |
| B£® | ĀČ»ÆĀĮČÜŅŗŗĶ¹żĮæµÄ°±Ė®·“Ó¦£ŗAl3++4NH3•H2OØTAl2-+4NH4++2H2O | |
| C£® | Ģ¼ĖįÄĘČÜŅŗÖŠ¼ÓČė¹żĮæ±½·Ó£ŗ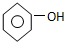 +CO32-”ś +CO32-”ś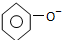 +HCO3- +HCO3- | |
| D£® | “ĪĀČĖįøĘČÜŅŗÖŠĶØČė¹żĮæCO2£ŗClO-+CO2+H2OØTHClO+HCO3- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
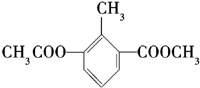
| A£® | Ņ»øö·Ö×ÓÖŠŗ¬ÓŠ12øöHŌ×Ó | B£® | ±½»·ÉĻµÄŅ»ĀČ“śĪļÓŠ2ÖÖ | ||
| C£® | ŗ¬ÓŠŅ»ÖÖŗ¬Ńõ¹ŁÄÜĶÅ | D£® | ·Ö×ÓŹ½ŹĒC11H12O4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com