
| y |
| 4 |
| z |
| 2 |
 或
或 .
. ,
, ;
; ,故答案为:
,故答案为: ;
;| 8 |
| 4 |
| 3 |
| 2 |
 或
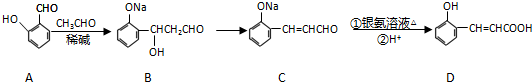
或 ,则X在NaOH醇溶液中反应的化学方程式为:
,则X在NaOH醇溶液中反应的化学方程式为: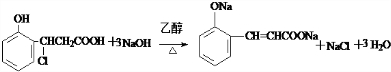 或
或 ,
, 或
或 .
.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、根据酸分子中含氢原子个数将酸分为一元酸、二元酸等 |
| B、根据反应中是否有电子的转移将化学反应分为氧化还原反应和非氧化还原反应 |
| C、根据电解质在熔融状态下能否完全电离将电解质分为强电解质和弱电解质 |
| D、根据元素原子最外层电子数的多少将元素分为金属和非金属 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、熔融烧碱时,不能使用普通石英坩埚:SiO2+2NaOH
| ||||
| B、AlCl3溶液中通入过量的NH3:Al3++4NH3?H2O=AlO2-+4NH4+ | ||||
C、红热的铁丝与水接触,表面形成蓝黑色(或黑色)保护层:3Fe+4H2O(g)
| ||||
| D、“84消毒液”(有效成分NaClO)和“洁厕灵”(主要成分盐酸)混合使用放出氯气:ClO-+Cl-+2H+=Cl2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 实验室以废铜屑为原料制取碱式碳酸铜【Cu2(OH)2CO3】的步骤如下:
实验室以废铜屑为原料制取碱式碳酸铜【Cu2(OH)2CO3】的步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 抗酸药X 【药品名称】:X 规格:2g:0.5g,2g/袋×20袋/盒 【用法用量】:直接口服或温水冲服,1~2袋/次,3~4次/天.除非另有医嘱,一般成人在餐后1~2小时、睡前或胃不适时服用.病情严重者遵医嘱增加剂量.儿童遵医嘱服用.治疗胃和十二指肠溃疡时,在症状缓解后,至少维持4周. 【适应症】:1.急、慢性胃炎.2.胃、十二脂肠溃疡.3.反流性食管炎.4.与胃酸有关的胃部不适症状,如胃痛、胃灼烧、酸性暖气、饱胀等.5.预防非甾体类药物引起的胃粘膜损伤. |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 时间/min | CH4(mol) | H2O(mol) | CO(mol) | H2(mol) |
| 0 | 0.40 | 1.00 | 0 | 0 |
| 5 | x1 | 0.80 | x2 | 0.60 |
| 7 | 0.20 | y1 | 0.20 | y2 |
| 10 | 0.21 | 0.81 | 0.19 | 0.64 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com