
 Ԫ��X��Y��ZΪǰ������Ԫ�أ�X�Ļ�̬ԭ�Ӻ��������21���˶�״̬��Ԫ��Y��ԭ�����������������ڲ��3����Z��X��Y����ͬһ���ڣ���Zԭ�Ӻ���p���ӱ�s���Ӷ�5����
Ԫ��X��Y��ZΪǰ������Ԫ�أ�X�Ļ�̬ԭ�Ӻ��������21���˶�״̬��Ԫ��Y��ԭ�����������������ڲ��3����Z��X��Y����ͬһ���ڣ���Zԭ�Ӻ���p���ӱ�s���Ӷ�5���� ���ѻ����ɱ��ͱ�ϩ��
���ѻ����ɱ��ͱ�ϩ������ Ԫ��X��Y��ZΪǰ������Ԫ�أ�X�Ļ�̬ԭ�Ӻ��������21���˶�״̬����X��ԭ������Ϊ21��ΪScԪ�أ�Ԫ��Y��ԭ�����������������ڲ��3����������������8�����ӣ���Y����2�����Ӳ㣬����㺬��6�����ӣ�ΪOԪ�أ�Z��X��Y����ͬһ���ڣ���Zλ�ڵ�һ��������ڣ���Zԭ�Ӻ���p���ӱ�s���Ӷ�5������Zֻ��λ�ڵ������ڣ���������Ų�ʽΪ1s22s22p63s23p5��ΪClԪ�أ��ݴ˽��н��
��� �⣺Ԫ��X��Y��ZΪǰ������Ԫ�أ�X�Ļ�̬ԭ�Ӻ��������21���˶�״̬����X��ԭ������Ϊ21��ΪScԪ�أ�Ԫ��Y��ԭ�����������������ڲ��3����������������8�����ӣ���Y����2�����Ӳ㣬����㺬��6�����ӣ�ΪOԪ�أ�Z��X��Y����ͬһ���ڣ���Zλ�ڵ�һ��������ڣ���Zԭ�Ӻ���p���ӱ�s���Ӷ�5������Zֻ��λ�ڵ������ڣ���������Ų�ʽΪ1s22s22p63s23p5��ΪClԪ�أ�
��1��X��ԭ������Ϊ21�����ݹ���ԭ�����������Ų�ʽΪ��[Ar]3d14s2��
�ʴ�Ϊ��[Ar]3d14s2��
��2���ٱ������к���6��C-C�Ҽ���6��C-H�Ҽ����ܹ�����12���Ҽ�����1mol�������к���12mol�Ҽ���
�ʴ�Ϊ��12��
�� �����б����ϵ�̼Ϊƽ��ṹ������sp2�ӻ������Ǽ��ͼ��ϵ�̼����sp3�ӻ�������̼ԭ�ӹ�����ӻ�������sp2��sp3��
�����б����ϵ�̼Ϊƽ��ṹ������sp2�ӻ������Ǽ��ͼ��ϵ�̼����sp3�ӻ�������̼ԭ�ӹ�����ӻ�������sp2��sp3��
�ʴ�Ϊ��sp2��sp3��
��3��Y3ΪO3��O3�ĵ�����Ϊ24������3��ԭ�ӣ�����O3���ӻ�Ϊ�ȵ������������ΪClO2+��
�ʴ�Ϊ��ClO2+��
��4��XZ3ΪScCl3��ScCl3������ˮ���۵�Ϊ960�棬����״̬���ܹ����磬˵������״̬���ܹ�������������ӣ���ScCl3Ϊ���ӻ�����������Ӿ��壬
�ʴ�Ϊ�����Ӿ��壻
��5��YΪOԪ�أ�����ͼʾ��֪���þ����к���8��Oԭ�ӣ�����Ceԭ�ӵ���ĿΪ��8��$\frac{1}{8}$+6��$\frac{1}{2}$=4����û�����Ļ�ѧʽΪ��CeO2��
�ʴ�Ϊ��CeO2��
���� ���⿼���Ϊ�ۺϣ��漰�������㡢Ԫ���ƶϡ�ԭ���ӻ���֪ʶ����Ŀ�Ѷ��еȣ��ƶ�Ԫ��Ϊ���ؼ���ע�����վ�̯���ھ��������е�Ӧ�ã�����������ѧ���ķ����������ۺ�Ӧ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 ��
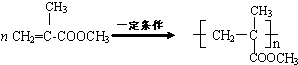
�� ������n����;���������ᣨ��дһ�ּ��ɣ���
������n����;���������ᣨ��дһ�ּ��ɣ����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʱ��t/h | 0 | 5 | 10 | 15 | �� | 25 | 30 |
| ��ѹǿp/100kPa | P0 | 1.5P0 | 1.75P0 | 1.875P0 | �� | 1.95P0 | 1.95P0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������


 ��E�к��������ŵ�����Ϊ�ǻ���̼̼������
��E�к��������ŵ�����Ϊ�ǻ���̼̼������ ��
�� ��
�� ����дһ�֣���F������ͬ���칹��������һ�ֱ�����������ʾ���źţ������ݣ���ȫ��ͬ����������d������ĸ����
����дһ�֣���F������ͬ���칹��������һ�ֱ�����������ʾ���źţ������ݣ���ȫ��ͬ����������d������ĸ���� �������Լ���ѡ��
�������Լ���ѡ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
 A��B��C��D��E��F��G����ǰ������Ԫ����ԭ��������������A��������ۺ�����۵ľ���ֵ��ȣ�B�Ļ�̬ԭ����3����ͬ���ܼ��Ҹ��ܼ��е�������ȣ�D�Ļ�̬ԭ����B�Ļ�̬ԭ�ӵ�δ�ɶԵ�����Ŀ��ͬ��E�Ļ�̬ԭ��s�ܼ��ĵ���������p�ܼ��ĵ�������ȣ�F�Ļ�̬ԭ�ӵ�3d�����������4s��������4����G2+��3d�����9�����ӣ���ش��������⣺
A��B��C��D��E��F��G����ǰ������Ԫ����ԭ��������������A��������ۺ�����۵ľ���ֵ��ȣ�B�Ļ�̬ԭ����3����ͬ���ܼ��Ҹ��ܼ��е�������ȣ�D�Ļ�̬ԭ����B�Ļ�̬ԭ�ӵ�δ�ɶԵ�����Ŀ��ͬ��E�Ļ�̬ԭ��s�ܼ��ĵ���������p�ܼ��ĵ�������ȣ�F�Ļ�̬ԭ�ӵ�3d�����������4s��������4����G2+��3d�����9�����ӣ���ش��������⣺
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 b��
b��
 d��
d��
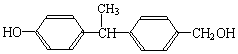
 �ṹ���ƵĴ����ܱ�����Ϊȩ���ᣮ
�ṹ���ƵĴ����ܱ�����Ϊȩ���ᣮ
 ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com