BD
分析:A、溴乙烷中不存在溴离子.
B、乙酸的酸性比碳酸酸性强,利用强酸制备弱酸原理.
C、醇发生催化氧化发生断键位置为羟基中的O-D键、与羟基相连的碳原子相邻的碳原子上的C-H键.
D、乙醛被氧化为乙酸,乙酸与碱反应生成盐.
解答:A、溴乙烷中不存在溴离子,无法只滴入AgNO
3溶液检验其中的溴元素,可先将溴乙烷水解再检验,故A错误;
B、醋酸酸性比碳酸酸性强,醋酸与碳酸钙反应生成醋酸钙、水、二氧化碳,
反应离子方程式为CaCO
3+2CH
3COOH=2CH
3COO
-+Ca
2++H
2O+CO
2↑,故B正确;
C、醇发生催化氧化发生断键位置为羟基中的O-D键、与羟基相连的碳原子相邻的碳原子上的C-H键,氘原子存在水中,故C错误;
D、乙醛被氧化为乙酸,乙酸与碱反应生成盐,所以乙醛溶液与足量的新制Cu(OH)
2悬浊液共热发生反应:CH
3CHO+2Cu(OH)
2+OH
-
CH
3COO
-+Cu
2O↓+3H
2O,故D正确.
故选:BD.
点评:考查醇、羧酸、醛性质及反应方程式书写,难度中等,D选项容易忽略生成的羧酸与碱反应,注意醇的氧化.

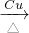 2CH3CDO+2H2O
2CH3CDO+2H2O CH3COO-+Cu2O↓+3H2O
CH3COO-+Cu2O↓+3H2O CH3COO-+Cu2O↓+3H2O,故D正确.
CH3COO-+Cu2O↓+3H2O,故D正确.

 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案