
焦硫酸(H2SO4·SO3)溶于水,其中的SO3都转化为硫酸。若将445 g焦硫酸溶于水配成4.00 L硫酸,该硫酸的物质的量浓度为________ mol·L-1。
科目:高中化学 来源: 题型:
3t℃时,水的离子积为 Kw,该温度下将a mol/L一元酸HA与b mol/L一元碱 BOH等体积混合,若混合后溶液呈中性,下列说法一定正确的是( )
A.混合液中,=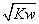 B.混合液的pH=7
B.混合液的pH=7
C.a=b D.混合液中,c(B+)=c(A-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
硫酸铜在生产、生活中应用广泛。某化工厂用含少量铁的废铜渣为原料生产胆矾的流程如下:
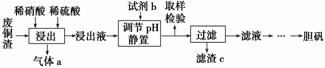
(1)写出浸出时铜与稀硫酸、稀硝酸反应生成硫酸铜的化学方程式:________________。
(2)取样检验是为了确认Fe3+是否除净,你的检验方法是____________。
(3)滤渣c是__________。
(4)气体a可以被循环利用,用化学方程式表示气体a被循环利用的原理为2NO+O2===2NO2、____________。
(5)一定温度下,硫酸铜受热分解生成CuO、SO2气体、SO3气体和O2气体,且n(SO3)∶n(SO2)=1∶2,写出硫酸铜受热分解的化学方程式:________________。
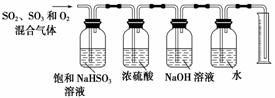
某同学设计了如下图所示的实验装置分别测定生成的SO2、SO3气体的质量和O2气体的体积。此设计有不合理之处,请说明理由:______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
海洋是一个丰富的资源宝库,通过海水的综合利用可获得许多物质供人类使用。
(1)海水中盐的开发利用:
①海水制盐目前以盐田法为主,建盐田必须选在远离江河入海口,多风少雨,潮汐落差大且又平坦空旷的海滩。所建盐田分为贮水池、 池和结晶池。
②工业上通常以NaCl 、CO2 和 NH3 为原料制取纯碱,请写出第一步制取NaHCO3的化学方程式:
(2)电渗析法是近年来发展起来的一种较好的海水淡化技术,其原理如图所示。其中具有选择性的阴离子交换膜和阳离子交换膜相间排列。请回答下面的问题:
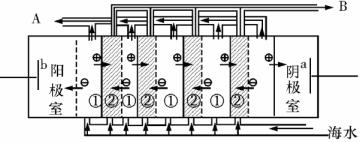
ⅰ电渗析法淡化海水中阴极室可获得的重要化工原料有
ⅱ上图中虚线部分表示 离子交换膜。 淡水从 (A或B) 排出。
(3)用苦卤(含Na+、K+、Mg2+、Cl-、Br-等离子)可提取溴,其生产流程如下:
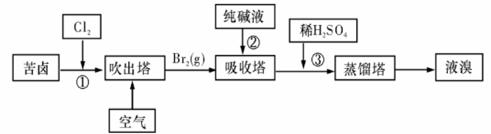
ⅰ写出反应③的离子方程式为: 。
ⅱ通过①氯化已获得含Br2的溶液,为何还需经过吹出、吸收、酸化来重新获得含Br2的溶液?
ⅲ向蒸馏塔中通入水蒸气加热,控制温度在90℃左右进行蒸馏的原因是
。
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值。下列有关叙述正确的是( )
A.在0 ℃时,22.4 L氢气中含有2NA个氢原子
B.电解食盐水若产生2 g氢气,则转移的电子数目为NA
C.1 mol乙烷分子中共价键总数为7NA
D.密闭容器中46 g NO2含有的分子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
某硫酸镁和硫酸铝的混合溶液中,c(Mg2+)=2 mol·L-1,c(SO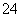 )=6.5 mol·L-1,若将200 mL此混合液中的Mg2+和Al3+ 分离,至少应加入1.6 mol·L-1的苛性钠溶液( )
)=6.5 mol·L-1,若将200 mL此混合液中的Mg2+和Al3+ 分离,至少应加入1.6 mol·L-1的苛性钠溶液( )
A.0.5 L B.1.625 L
C.1.8 L D.2 L
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列各溶液的叙述中正确的是
A. NaHSO3与Na2SO3混合溶液中:3c(Na+)=c(HSO3-)+c(SO32-)
B. 0.1 mol/L 的醋酸钠溶液20 mL与0.1 mol/L盐酸10mL 混合后溶液显酸性:
c(CH3COO-)>c(CH3COOH)>c(Cl-)>c(H+)
C. 等物质的量浓度等体积的NH4HSO4和NaOH溶液混合:
c(Na+)=c(SO42-) >c ( NH4+)> c(H+)>c(OH-)
D. 向1.00L 0.3 mol/L NaOH溶液中缓慢通入0.2 mol CO2气体,溶液中:
c(Na+)>c(CO32-) >c(HCO3-)>c(OH-)> c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com