
科目:高中化学 来源: 题型:实验题
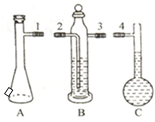 在“测定1mol气体体积”实验中,我们通常选择的测量气体是氢气,选择的反应原理是镁和稀硫酸反应.
在“测定1mol气体体积”实验中,我们通常选择的测量气体是氢气,选择的反应原理是镁和稀硫酸反应.| 实验次数 | 镁带质量(g) | 硫酸体积(mL) | C瓶读数(mL) | 抽出气体的体积(mL) |
| 1 | 0.108 | 10.0 | 129.2 | 8.0 |
| 2 | 0.105 | 10.0 | 125.7 | 6.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 空气(混合物)、C2H5OH(醇)、H2SO4(离子化合物)、CO2(非电解质) | |
| B. | HCl(共价化合物)、CH3COOH(羧酸)、Na2O2(碱性氧化物)、CH3I(卤代烃) | |
| C. | 液氨(氢化物)、NH4Cl(铵盐)、HNO3(含氧酸)、NaOH(强电解质) | |
| D. | NO2(酸性氧化物)、CH3CHO(有机物)、CO(有机物)、CH3COOCH3(酯) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有H+的溶液呈酸性 | |
| B. | 能使红色石蕊试纸显蓝色的溶液为酸性溶液 | |
| C. | pH=7的溶液为中性溶液 | |
| D. | 等物质的量浓度、等体积的NaOH溶液和醋酸混合后溶液呈碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 小苏打中加入过量的澄清石灰水:Ca2++2OH-+2HCO3-═CaCO3↓+2H2O+CO32- | |
| B. | 偏铝酸钠溶液中通入过量的CO2:CO2+3H2O+2AlO2-═2Al(OH)3↓+CO32- | |
| C. | Na2SO3溶液使酸性KMnO4溶液褪色:5SO32-+6H++2MnO4-═5SO42-+2Mn2++3H2O | |
| D. | Fe(NO3)2溶液中加入过量的HI溶液:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 上述两溶液中盐酸的物质的量浓度比硫酸的物质的量浓度大 | |
| B. | 硫酸使铝钝化 | |
| C. | 生成的氯化铝能溶于水,而生成的硫酸铝难溶于水 | |
| D. | 氯离子可能破坏氧化铝薄膜,而硫酸根离子不能 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com