
| A. | 仅HCl | B. | 只有HCl和HClO | C. | 只有HCl和Cl2 | D. | HCl、HClO和Cl2 |
科目:高中化学 来源: 题型:选择题
| 诜项 | 实验操作 | 实验目的 |
| A | 将乙烯通入酸性KMnO4溶液中 | 证明乙烯能发生加成反应 |
| B | 向含酚酞的NaOH溶液中加入氯水 | 证明Cl2具有漂白性 |
| C | 常温下,向Fe和Cu中分别加入浓硝酸 | 比较Fe和Cu的金属活动性 |
| D | 将铁钉放入试管中,下端浸入食盐水中 | 验证铁的吸氧腐蚀 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
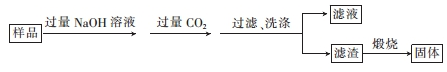
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若HA、HB均为弱酸,酸性:HA>HB,则相同条件下,溶液的pH大小为NaA>NaB | |
| B. | 相同条件下,将pH=11的NaOH溶液和和氨水分别稀释pH=9的溶液,所加水的体积前者大 | |
| C. | pH=3的醋酸与pH=1的NaOH溶液等体积混合时,溶液中离子浓度的大小顺序是:c(Na+)>c(CHCOO-)>c(OH-)>c(H+) | |
| D. | 0.1mol/L的某二元弱酸盐Na2A溶液中,c(Na+)=2[c(HA-)+c(A2-)+c(H2A)] |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第一电离能:Y<X | |
| B. | 最简单气态氢化物的稳定性:HmY>HnX | |
| C. | 最高价含氧酸的酸性:元素X对应酸的酸性强于Y | |
| D. | X和Y形成的化合物中,X显负价,Y显正价 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯原子的结构示意图: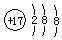 | B. | 甲烷分子的球棍模型: | ||
| C. | 氯化镁的电子式: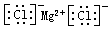 | D. | 原子核内有8个中子的氧原子:818O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在NaOH溶液中滴入几滴NH4Cl溶液:NH4++OH-═NH3↑+H2O | |
| B. | 氟气通入水中:2F2+2H2O═4H++4F-+O2 | |
| C. | AlCl3溶液中通入过量的氨气:Al3++3NH3•H2O═Al(OH)3↓+3NH${\;}_{4}^{+}$ | |
| D. | 将少量铜屑放入浓硝酸中:Cu+4 H++2NO3-═Cu2++2 NO2↑+2 H2O |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高一上10月月考化学试卷(解析版) 题型:选择题
用容量瓶配制一定物质的量浓度的溶液,该容量瓶必须是( )
A. 干燥的 B. 不漏水的
C. 用欲配制的溶液润洗过的 D. 以上三项均需要求
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二上教学质检化学试卷(解析版) 题型:填空题
A、B、C、D、E是五种短周期元素,F是过渡元素。A、B、C、E同周期,C、D同主族,A元素在地壳含量中排名第二,B是同周期第一电离能最小的元素,C原子的最外层有三个未成对电子,E单质常温下为淡黄色固体,F的外围电子排布式为3d64s2。回答下列问题:
(1)写出下列元素的名称:A B 。
(2)B、C、E第一电离能由大到小的顺序是 (用元素符号作答)。
(3)写出D元素原子构成单质的电子式 ,D的简单气态氢化物的空间构型为 。
(4)F元素在周期表中的位置为 ,其形成的简单离子F3+的核外电子排布式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com