
分析 (1)氨气分解为熵增的反应,根据△G=△H-T△S<0,反应可以自发进行;
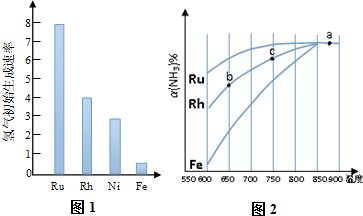
(2)反应的活化能越高,则反应中活化分子数越少,反应速率越慢;
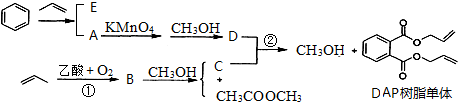
(3)①850°以后氨气的转化率不变,说明a点处于平衡状态;
②b、c点均未达到平衡,c点温度较高,反应速率较快;
③Ni催化分解氨气,平衡时α(NH3)不变,Ni的催化效率高于Fe、小于Rh,一定温度下,氨气的转化率应大于Fe、小于Rh;
④根据氨气的转化率,计算平衡时氨气浓度变化量,利用三段式计算平衡时各组分的浓度,代入平衡常数表达式K=$\frac{c({N}_{2})×{c}^{3}({H}_{3})}{{c}^{2}(N{H}_{3})}$计算;
(4)液氨中氨气发生微弱电离得到NH2-与NH4+,阴极发生还原反应,类比水的电解,可知阴极上NH3获得电子生成H2与NH2-.
解答 解:(1)△G=△H-T△S<0,反应可以自发进行,氨气分解为熵增的反应,且△H为增大反应,故反应在高温下可以自发进行,
故答案为:高温;
(2)反应的活化能越高,则反应中活化分子数越少,反应速率越慢,则氨气的分解速率最慢的反应中,氨气分解反应的活化能最大,即当Fe作催化剂时活化能最大,
故答案为:Fe;
(3)①850°以后氨气的转化率不变,说明a点处于平衡状态,故答案为:是;
②b、c点均未达到平衡,c点温度较高,反应速率较快,氨气的转化率较高,
故答案为:b、c点均未达到平衡,c点温度较高,反应速率较快,氨气的转化率较高;
③Ni催化分解氨气,平衡时α(NH3)不变,Ni的催化效率高于Fe、小于Rh,一定温度下,氨气的转化率应大于Fe、小于Rh,故Ni催化分解氨气过程的总趋势曲线为 ,
,
故答案为: ;
;
④氨气的初始浓度为c0,平衡转化率为40%,则平衡时氨气浓度变化量为0.4c0,则:
2NH3(g)?N2 (g)+3H2(g)
开始(mol/L):c0 0 0
转化(mol/L):0.4c0 0.2c0 0.6c0
平衡(mol/L):0.6c0 0.2c00.6c0
故平衡常数表达式K=$\frac{c({N}_{2})×{c}^{3}({H}_{3})}{{c}^{2}(N{H}_{3})}$=$\frac{0.2{c}_{0}×(0.6{c}_{0})^{3}}{(0.6{c}_{0})^{2}}$=0.12 c02,
故答案为:0.12 c02;
(4)液氨中氨气发生微弱电离得到NH2-与NH4+,阴极发生还原反应,类比水的电解,可知阴极上NH3获得电子生成H2与NH2-,阴极的电极反应式是:2NH3+2e-=H2↑+2NH2-,
故答案为:2NH3+2e-=H2↑+2NH2-.
点评 本题考查反应自发性判断、化学反应速率及化学平衡影响因素、平衡常数计算、电解原理,侧重考查学生的分析能力、对知识的应用能力,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | H+(aq)+$\frac{1}{2}$SO42-(aq)+$\frac{1}{2}$Ba2+(aq)+OH-(aq)═$\frac{1}{2}$BaSO4(s)+H2O(1);△H=-57.3 kJ/mol | |
| B. | KOH(aq)+$\frac{1}{2}$H2SO4(aq)═$\frac{1}{2}$K2SO4(aq)+H2O(l);△H=-57.3kJ/mol | |
| C. | C8H18(l)+$\frac{25}{2}$O2 (g)═8CO2 (g)+9H2O(g);△H=-5518 kJ/mol | |
| D. | 2C8H18(g)+25O2 (g)═16CO2 (g)+18H2O(1);△H=-5518 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2和CaO的熔化 | B. | 氧化钠和铁的熔化 | ||
| C. | 碘和干冰的气化 | D. | 晶体硅和晶体硫的熔化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
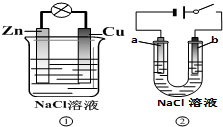
| A. | 装置①中的铜棒上冒气泡 | |
| B. | 若b是惰性电极,则装置②中的a、b 冒气泡 | |
| C. | 装置①换上硫酸铜溶液,将实现锌片上镀铜 | |
| D. | 装置②换上硫酸铜溶液,将实现“b极”镀铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容量瓶、量筒和滴定管上都标有使用温度,量筒、容量瓶无“0”刻度,滴定管有“0”刻度;使用时滴定管水洗后还需润洗,但容量瓶水洗后不用润洗 | |
| B. | 在用简易量热计测定反应热时,可使用碎泡沫起隔热保温的作用、普通玻璃棒进行搅拌使酸和碱充分反应、准确读取实验时温度计最高温度、并且取2-3 次的实验平均值等措施,以达到良好的实验效果 | |
| C. | 金属着火时,可用细沙覆盖灭火;电器设备引起的火灾,不可用泡沫灭火器灭火 | |
| D. | 在4mL0.1mol•L-1的K2Cr2O7溶液中滴加数滴1mol•L-1的NaOH溶液,溶液颜色从橙色变成黄色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 组别 | 甲 | 乙 | 丙 |
| A | SO2 | Ba(OH)2 | NaHCO3 |
| B | Na2O2 | H2O | CO2 |
| C | Na2SiO3 | NaOH | HCl |
| D | Al | H2SO4 | NaOH |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| n(SO32-):n(HSO3-) | 91.9 | 1:1 | 1:91 |
| pH | 8.2 | 7.2 | 6.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+、Cu2+、Fe3+、SO42- | B. | Na+、Ba2+、Al3+、Cl- | ||
| C. | K+、Ag+、NH4+、NO3- | D. | Na+、K+、Br-、OH- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com