
�״���һ�ֺܺõ�ȼ�ϣ���ҵ����CH4��H2O Ϊԭ�ϣ�ͨ����ӦI�͢����Ʊ��״���
�Ž�1.0 mol CH4��2.0 mol H2O(g)ͨ�˷�Ӧ��(�ݻ�Ϊ100L)����һ�������·�����Ӧ:
CH4(g)��H2O(g) CO(g)��3H2(g)����I��CH4��ת�������¶ȡ�ѹǿ�Ĺ�ϵ����ͼ��ʾ��
CO(g)��3H2(g)����I��CH4��ת�������¶ȡ�ѹǿ�Ĺ�ϵ����ͼ��ʾ��
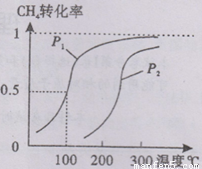
����֪100��ʱ�ﵽƽ�������ʱ��Ϊ5min������H2��ʾ��ƽ����Ӧ����Ϊ ��
��ͼ�е�P1_ P2(�<������>����=��),100��ʱƽ�ⳣ��Ϊ ��
�۸÷�Ӧ�ġ�H 0(�<������>����=��)��
(2)��һ�������£���a mol CO��3a mol H2�Ļ�������ڴ������������Է���Ӧ���ɼ״�: CO(g)+2H2(g) CH3OH(g)
��H<0 ������
CH3OH(g)
��H<0 ������
���������ݻ����䣬���д�ʩ�����Ӽ״����ʵ���
A�������¶� B����CH3OH(g)����ϵ�з���
C������He��ʹ��ϵ��ѹǿ���� D���ٳ���lmol CO��3 mol H2
��Ϊ��Ѱ�Һϳɼ״����¶Ⱥ�ѹǿ������������ijͬѧ���������ʵ�飬����ʵ�������Ѿ���������ʵ����Ʊ��С�
A���±���ʣ���ʵ����������: a=_ ��b=_ ��
|
ʵ���� |
T���棩 |
n(CO)��n(H2) |
P(Mpa) |
|
1 |
150 |
1��3 |
0.1 |
|
2 |
a |
1��3 |
5 |
|
3 |
350 |
b |
5 |
B�����ݷ�Ӧ����ص㣬����ͼ����ѹǿ�ֱ�Ϊ0.1 MPa��5MPa��CO��ת�������¶ȱ仯������ͼ����ָ��ͼ�е�ѹǿPx = Mpa��

��14�֣���1����0.0030mol/(L��min) ��2�֣� �ڣ� ��2�֣�
2.25��10��4(mol/L)2��2�֣���д��λ���۷֣���λд����1�֣� �ۣ���2�֣�
��2����BD��2�֣�
��A.a��150��b��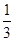 ����1�֣���2�֣� B.0.1��2�֣�
����1�֣���2�֣� B.0.1��2�֣�
��������
�����������1������ͼ���֪��ƽ��ʱ�����ת����Ϊ0.5�����Լ�������ʵ���������1.5mol��0.5��0.5mol�����c(CH4)��0.5mol��100L��0.005mol/L������v(CH4)��0.005mol/L��5min��0.001mol/��L•min��������֮�ȵ��ڻ�ѧ������֮�ȣ�����v(H2)��3v(CH4)��3��0.001mol/��L•min��=0.003mol/��L•min����
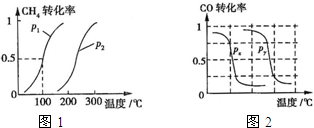
���¶���ͬʱ������ֱx��ĸ����ߣ�����ѹǿΪP1��CH4��ת���ʸߣ���ӦΪǰ���������ķ�Ӧ��ѹǿ����ƽ���������С�ķ����ƶ��������淴Ӧ�ƶ���CH4��ת���ʽ��ͣ�����P1��P2����
CH4��g���� H2O��g��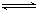 CO��g���� 3H2��g��
CO��g���� 3H2��g��
��ʼŨ�ȣ�mol/L�� 0.010 0.020 0 0
ת��Ũ�ȣ�mol/L�� 0.005 0.005 0.005 0.015
ƽ��Ũ�ȣ�mol/L�� 0.005 0.015 0.005 0.015
����ƽ�ⳣ��K��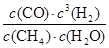 =
=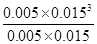 ��2.25��10-4��
��2.25��10-4��
����ͼ��֪���¶�Խ�����ת����Խ�������¶�ƽ��������Ӧ�����ƣ��¶�����ƽ�������ȷ����ƶ�����������ӦΪ���ȷ�Ӧ������H��0��
��2����A���÷�ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�������ȷ����ƶ��������淴Ӧ�����ƶ����״��IJ��ʽ��ͣ���A����B����CH3OH��g������ϵ�з��룬�����Ũ�Ƚ��ͣ�ƽ��������Ӧ�ƶ����״��IJ������ӣ���B����C������He��ʹ��ϵ��ѹǿ���������ݻ����䣬��Ӧ���������Ũ�Ȳ��䣬ƽ�ⲻ�ƶ����״��IJ��ʲ��䣬��C����D���ٳ���1molCO��3molH2���ɵ�ЧΪѹǿ����ƽ���������С�ķ����ƶ�����������Ӧ�����ƶ����״��IJ������ӣ���D��ȷ����ѡBD��
��A����ȡ���Ʊ�������̽���ϳɼ״����¶Ⱥ�ѹǿ�����������������¶ȡ�ѹǿ�DZ仯�ģ�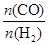 Ӧ���ֲ��䣬����b��
Ӧ���ֲ��䣬����b��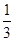 ���Ƚ�ʵ��1��2��֪��ѹǿ��ͬ�������¶�Ӧ��ͬ����a��150��
���Ƚ�ʵ��1��2��֪��ѹǿ��ͬ�������¶�Ӧ��ͬ����a��150��
B���¶���ͬʱ������ֱx��ĸ����ߣ�����ѹǿΪPy��CO��ת���ʸߣ���ӦΪǰ�������С�ķ�Ӧ��ѹǿ����ƽ���������С�ķ����ƶ�����������Ӧ�ƶ�������Px��Py�����ѹǿPx��0.1Mpa��
���㣺���鷴Ӧ���ʡ�ƽ�ⳣ���ļ��㣻���������ƽ��״̬��Ӱ���Լ�ͼ��ʶ���


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��2013?����ģ�⣩�״���һ�ֺܺõ�ȼ�ϣ���ҵ����CH4��H2OΪԭ�ϣ�ͨ��������Ӧ��͢����Ʊ��״���
��2013?����ģ�⣩�״���һ�ֺܺõ�ȼ�ϣ���ҵ����CH4��H2OΪԭ�ϣ�ͨ��������Ӧ��͢����Ʊ��״���| ʵ���� | T���棩 | n��CO��/n��H2�� | p��MPa�� | ||
| l | 150 |
|
0.1 | ||
| 2 | n |
|
5 | ||
| 3 | 350 | m | 5 |
| 1 |
| 3 |
| 1 |
| 3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
 CH3OH��g����H1=-116kJ?mol��1
CH3OH��g����H1=-116kJ?mol��1| 1 |
| 2 |
| 1 |
| 2 |

| ʵ���� | T���棩 | n��CO��/n��H2�� | P��MPa�� |
| 1 | 150 | 1/3 | 0.1 |
| 2 | a | 1/3 | 5 |
| 3 | 350 | b | 5 |
 ��������ͼ����ָ��ͼ�е�ѹǿP1=
��������ͼ����ָ��ͼ�е�ѹǿP1= CO��g��+2H2��g����Ӧ��ƽ�ⳣ��Ϊ
CO��g��+2H2��g����Ӧ��ƽ�ⳣ��Ϊ| 4a2 |
| V2 |
| 4a2 |
| V2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �״���һ�ֺܺõ�ȼ�ϣ���ҵ����CH4��H2O��g��Ϊԭ�ϣ�ͨ����Ӧ��͢����Ʊ��״�����ش��������⣺
�״���һ�ֺܺõ�ȼ�ϣ���ҵ����CH4��H2O��g��Ϊԭ�ϣ�ͨ����Ӧ��͢����Ʊ��״�����ش��������⣺| ʵ���� | T���棩 | n��CO��/n��H2�� | �ѣ�MPa�� | ||
| 1 | 150 |
|
0.1 | ||
| 2 | n |
|
5 | ||
| 3 | 350 | m | 5 |
| 1 |
| 3 |
| 1 |
| 3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�״���һ�ֺܺõ�ȼ�ϣ���ҵ����CH4��H2OΪԭ�ϣ�ͨ����Ӧ��͢����Ʊ��״���

�Ž�1.0 mol CH4��2.0 mol H2O(g)ͨ�뷴Ӧ�ң��ݻ�Ϊ100L������һ�������·�����Ӧ��
CH4��g��+H2O��g��![]() CO��g��+3H2��g��������CH4��ת�������¶ȡ�ѹǿ�Ĺ�ϵ����ͼ��
CO��g��+3H2��g��������CH4��ת�������¶ȡ�ѹǿ�Ĺ�ϵ����ͼ��
����֪100��ʱ�ﵽƽ�������ʱ��Ϊ5min������H2��ʾ��ƽ����Ӧ����Ϊ ��
��ͼ�е�P1 P2���<������>����=������100��ʱƽ�ⳣ��Ϊ ��
�۸÷�Ӧ�ġ�H 0���<������>����=������
����ѹǿΪ0.1 MPa�����£���a mol CO�� 3a mol H2�Ļ�������ڴ������������Է���Ӧ���ɼ״���CO��g��+2H2��g��![]() CH3OH��g������H<0������
CH3OH��g������H<0������
���������ݻ����䣬���д�ʩ�����Ӽ״����ʵ��� ��
A�������¶� B����CH3OH��g������ϵ�з���
C������He��ʹ��ϵ��ѹǿ���� D���ٳ���1mol CO��3mol H2
 ��Ϊ��Ѱ�Һϳɼ״����¶Ⱥ�ѹǿ������������ijͬѧ���������ʵ�飬����ʵ�������Ѿ���������ʵ����Ʊ��С�
��Ϊ��Ѱ�Һϳɼ״����¶Ⱥ�ѹǿ������������ijͬѧ���������ʵ�飬����ʵ�������Ѿ���������ʵ����Ʊ��С�

A�����ϱ���ʣ���ʵ���������ݣ�a=________��b=_______��
B�����ݷ�Ӧ����ص㣬����ͼ����ѹǿ�ֱ�Ϊ0.1MPa��5MPa��CO��ת�������¶ȱ仯������ͼ����ָ��ͼ�е�ѹǿPx=_________MPa��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011����������һ�и�����ѧ�ڵ�����¿������ۣ���ѧ���� ���ͣ������
�״���һ�ֺܺõ�ȼ�ϣ���ҵ����CH4��H2OΪԭ�ϣ�ͨ����Ӧ��͢����Ʊ��״���
��1����1.0 mol CH4��2.0 mol H2O(g)ͨ�뷴Ӧ�ң��ݻ�Ϊ100L������һ�������·�����Ӧ��
CH4(g)+H2O(g)  CO(g)+3H2(g)������
CO(g)+3H2(g)������
CH4��ת�������¶ȡ�ѹǿ�Ĺ�ϵ����ͼ��
����֪100��ʱ�ﵽƽ�������ʱ��Ϊ5min,����H2��ʾ��ƽ����Ӧ����Ϊ ��
��ͼ�е�P1 P2���<������>����=������100��ʱƽ�ⳣ��Ϊ ��
�۸÷�Ӧ�ġ�H 0(�<������>����=��)��
��2����ѹǿΪ0.1 MPa������, ��a mol CO�� 3a mol H2�Ļ�������ڴ������������Է���Ӧ���ɼ״���CO(g)+2H2(g)  CH3OH(g)����H<0������
CH3OH(g)����H<0������
���������ݻ����䣬���д�ʩ�����Ӽ״����ʵ��� ��
A�������¶� B����CH3OH(g)����ϵ�з���
C������He��ʹ��ϵ��ѹǿ���� D���ٳ���1mol CO��3mol H2
��Ϊ��Ѱ�Һϳɼ״����¶Ⱥ�ѹǿ������������ijͬѧ���������ʵ�飬����ʵ�������Ѿ���������ʵ����Ʊ��С�
A�����ϱ���ʣ���ʵ����������:a="________ " b=_______
B�����ݷ�Ӧ����ص㣬����ͼ����ѹǿ�ֱ�Ϊ0.1MPa��5MPa��CO��ת�������¶ȱ仯������ͼ����ָ��ͼ�е�ѹǿPx=_________MPa��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com